题目内容
某校化学研究性学习小组查阅资料了解到以下内容:
乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,易溶于水,属于二元中强酸(为弱电解质),且酸性强于碳酸,其熔点为101.5℃,在157℃升华.为探究草酸的部分化学性质,进行了如下实验:
(1)向盛有1mL饱和NaHCO3溶液的试管中加入足量乙二酸溶液,观察到有无色气泡产生.该反应的离子方程式为
(2)向盛有乙二酸饱和溶液的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现其溶液的紫红色褪去;①说明乙二酸具有
(3)将一定量的乙二酸放于试管中,按下图所示装置进行实验(夹持装置未标出):

实验发现:装置C、G中澄清石灰水变浑浊,B中CuSO4粉末变蓝,F中CuO粉末变红.据此回答:
①上述装置中,D的作用是
②乙二酸分解的化学方程式为
(4)该小组同学将2.52g草酸晶体(H2C2O4?2H2O)加入到100mL 0.2mol/L的NaOH溶液中充分反应,测得反应后溶液呈酸性,其原因是
乙二酸(HOOC-COOH,可简写为H2C2O4)俗称草酸,易溶于水,属于二元中强酸(为弱电解质),且酸性强于碳酸,其熔点为101.5℃,在157℃升华.为探究草酸的部分化学性质,进行了如下实验:
(1)向盛有1mL饱和NaHCO3溶液的试管中加入足量乙二酸溶液,观察到有无色气泡产生.该反应的离子方程式为
HCO3-+H2C2O4=HC2O4-+CO2↑+H2O
HCO3-+H2C2O4=HC2O4-+CO2↑+H2O
;(2)向盛有乙二酸饱和溶液的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现其溶液的紫红色褪去;①说明乙二酸具有
还原性
还原性
(填“氧化性”、“还原性”或“酸性”);②请配平该反应的离子方程式:2
2
MnO4-+5
5
H2C2O4+6
6
H+=2
2
Mn2++10
10
CO2↑+8
8
H2O(3)将一定量的乙二酸放于试管中,按下图所示装置进行实验(夹持装置未标出):

实验发现:装置C、G中澄清石灰水变浑浊,B中CuSO4粉末变蓝,F中CuO粉末变红.据此回答:
①上述装置中,D的作用是
除去混合气体中的CO2
除去混合气体中的CO2
,②乙二酸分解的化学方程式为
H2C2O4
H2O+CO↑+CO2↑
| ||
H2C2O4
H2O+CO↑+CO2↑
;
| ||
(4)该小组同学将2.52g草酸晶体(H2C2O4?2H2O)加入到100mL 0.2mol/L的NaOH溶液中充分反应,测得反应后溶液呈酸性,其原因是
反应所得溶液为NaHC2O4溶液,由于HC2O4-的电离程度比水解程度大,导致溶液中c(H+)>c(OH-),所以溶液呈酸性
反应所得溶液为NaHC2O4溶液,由于HC2O4-的电离程度比水解程度大,导致溶液中c(H+)>c(OH-),所以溶液呈酸性
(用文字简单表述),该溶液中各离子的浓度由大到小的顺序为:Na+>HC2O4->H+>C2O42->OH-
Na+>HC2O4->H+>C2O42->OH-
(用离子符号表示).分析:(1)由于题中强调足量的草酸,故反应后草酸转化为HC2O4-,若写成C2O42-是错误的.
(2)中显然说明草酸具有还原性,把MnO4-还原为Mn2+,根据氧化还原反应得失电子守恒配平反应方程式;
(3)乙二酸分解的化学方程式为H2C2O4
H2O+CO↑+CO2↑,由各物质的性质可推测B中CuSO4固体检验草酸分解产物中的水,C装置检验草酸分解产物中的CO2,D装置的目的是为了除尽CO2,防止影响后续实验现象的判断,E装置用来干燥气体,F、G装置用来判断草酸分解产物中有无CO生成.
(4)两者正好1:1反应生成NaHC2O4,溶液显酸性说明HC2O4-的电离程度大于其水解程度,可得离子浓度间的大小关系.
(2)中显然说明草酸具有还原性,把MnO4-还原为Mn2+,根据氧化还原反应得失电子守恒配平反应方程式;
(3)乙二酸分解的化学方程式为H2C2O4
| ||
(4)两者正好1:1反应生成NaHC2O4,溶液显酸性说明HC2O4-的电离程度大于其水解程度,可得离子浓度间的大小关系.
解答:解:(1)题中强调足量的草酸,故反应后草酸转化为HC2O4-,且酸性强于碳酸,
反应的离子方程式为HCO3-+H2C2O4=HC2O4-+CO2↑+H2O,故答案为:HCO3-+H2C2O4=HC2O4-+CO2↑+H2O;
(2)①向盛有乙二酸饱和溶液的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现其溶液的紫红色褪去,说明具有氧化性的高锰酸钾被还原,说明草酸具有还原性,把MnO4-还原为Mn2+,故答案为:还原性;
②反应中根据氧化剂得失电子守恒可知氧化剂和还原剂物质的量之间的关系为:2MnO4-~5H2C2O4,在根据电荷守恒和质量守恒可写出反应方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,故答案为:2;5;6;2;10;8;
(3)①乙二酸分解的化学方程式为H2C2O4
H2O+CO↑+CO2↑,由各物质的性质可推测B中CuSO4固体检验草酸分解产物中的水,C装置检验草酸分解产物中的CO2,D装置的目的是为了除尽CO2,防止影响后续实验现象的判断,E装置用来干燥气体,F、G装置用来判断草酸分解产物中有无CO生成,故答案为:除去混合气体中的CO2;
②根据题意知草酸分解生成一氧化碳、二氧化碳和水,反应方程式为H2C2O4
H2O+CO↑+CO2↑,
故答案为:H2C2O4
H2O+CO↑+CO2↑;
(4)两者正好1:1反应生成NaHC2O4,溶液显酸性说明HC2O4-的电离程度大于其水解程度,而溶液中还存在着水的电离,故H+>C2O42-,由于离子的电离程度较小,则有HC2O4->H+,故正确顺序为Na+>HC2O4->H+>C2O42->OH-,
故答案为:反应所得溶液为NaHC2O4溶液,由于HC2O4-的电离程度比水解程度大,导致溶液中c(H+)>c(OH-),所以溶液呈酸性;Na+>HC2O4->H+>C2O42->OH-.
反应的离子方程式为HCO3-+H2C2O4=HC2O4-+CO2↑+H2O,故答案为:HCO3-+H2C2O4=HC2O4-+CO2↑+H2O;
(2)①向盛有乙二酸饱和溶液的试管中滴入几滴硫酸酸化的KMnO4溶液,振荡,发现其溶液的紫红色褪去,说明具有氧化性的高锰酸钾被还原,说明草酸具有还原性,把MnO4-还原为Mn2+,故答案为:还原性;
②反应中根据氧化剂得失电子守恒可知氧化剂和还原剂物质的量之间的关系为:2MnO4-~5H2C2O4,在根据电荷守恒和质量守恒可写出反应方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,故答案为:2;5;6;2;10;8;
(3)①乙二酸分解的化学方程式为H2C2O4
| ||
②根据题意知草酸分解生成一氧化碳、二氧化碳和水,反应方程式为H2C2O4
| ||
故答案为:H2C2O4
| ||
(4)两者正好1:1反应生成NaHC2O4,溶液显酸性说明HC2O4-的电离程度大于其水解程度,而溶液中还存在着水的电离,故H+>C2O42-,由于离子的电离程度较小,则有HC2O4->H+,故正确顺序为Na+>HC2O4->H+>C2O42->OH-,
故答案为:反应所得溶液为NaHC2O4溶液,由于HC2O4-的电离程度比水解程度大,导致溶液中c(H+)>c(OH-),所以溶液呈酸性;Na+>HC2O4->H+>C2O42->OH-.
点评:本题考查已二酸的分解以及溶液离子浓度的大小比较,题目较为综合且具有一定难度,做题时注意抓住反应的现象,以此推断物质可能具有的性质.

练习册系列答案
 好成绩1加1期末冲刺100分系列答案
好成绩1加1期末冲刺100分系列答案 金状元绩优好卷系列答案
金状元绩优好卷系列答案
相关题目
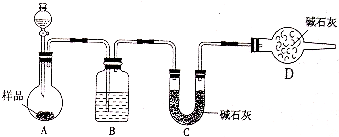
 某校化学研究性学习小组设计如下实验方案,测定放置己久的小苏打样品中纯碱的质量分数.
某校化学研究性学习小组设计如下实验方案,测定放置己久的小苏打样品中纯碱的质量分数.