题目内容
17.有质量分数为a的氨水溶液,蒸发掉原溶液质量一半的水后,浓度从C1mol/L变成C2mol/L,下列说法正确的是( )| A. | C2=2C1 | B. | C2>2C1 | C. | C2<2C1 | D. | C2=a |
分析 质量分数为a的氨水溶液,加入等质量的水稀释后,蒸发掉原溶液质量一半的水后,由于氨水的浓度越大密度越小,故浓缩后氨水的密度变小,根据c=$\frac{1000ρw}{M}$,计算氨水的物质的量浓度,据此判断.
解答 解:质量分数为a的氨水溶液,加入等质量的水稀释后,蒸发掉原溶液质量一半的水后,设质量分数a的氨水密度为ρ1g/ml,浓缩后氨水的为ρ2g/ml,
质量分数2a的氨水的物质量浓度为C1=$\frac{1000×{ρ}_{1}×a}{17}$mol/L,
稀释后氨水的物质量浓度为C2=$\frac{1000×{ρ}_{2}×2a}{17}$mol/L,
所以$\frac{{c}_{1}}{{c}_{2}}$=$\frac{{ρ}_{1}}{2{ρ}_{2}}$,由于氨水的浓度越大密度越小,故浓缩后氨水的密度变小,所以ρ1>ρ2,故所以C2<2C1,
故选:C.
点评 本题考查物质的量浓度的有关计算,难度中等,可利用定义计算浓度,关键理解物质的量浓度定义,注意氨水、酒精的浓度越大、密度越小.

练习册系列答案
相关题目
7.结晶玫瑰是具有强烈玫瑰香气的香料,可由如图反应路线合成:
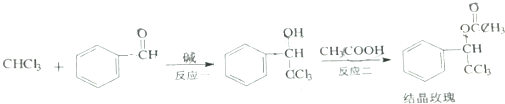
关于如图合成过程下列说法不正确的是( )

关于如图合成过程下列说法不正确的是( )
| A. | 反应一是加成反应 | |
| B. | 反应二的发生可用浓硫酸做催化剂 | |
| C. | 结晶玫瑰分子式为C10H9Cl3O2 | |
| D. | 上述过程中所有有机物的官能团共有6种 |
8.已知氯元素的近似相对原子质量为35.5,由23Na和35Cl及37Cl构成的25g纯NaCl中含Na35Cl的质量是( )
| A. | 18.75g | B. | 18.59g | C. | 26.1g | D. | 26.33g |
5.下列叙述正确的是( )
| A. | Na在氧气中燃烧主要生成Na2O | |
| B. | 将CO2通入次氯酸钙溶液可生成次氯酸 | |
| C. | 将SO2通入BaCl2溶液可生成BaSO3沉淀 | |
| D. | 将NH3通入热的CuSO4溶液中能使Cu2+还原成Cu |
9.油脂在人体内水解最终生成高级脂肪酸和( )
| A. | 乙醇 | B. | 葡萄糖 | C. | 甘油 | D. | 氨基酸 |
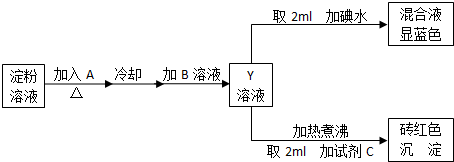
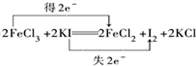 .向反应后的溶液中加入CCl4溶液,振荡、静置后会发现下层液体的颜色为紫色,再将混合液倒入分液漏斗(填仪器名称)中,将两层液体分离.
.向反应后的溶液中加入CCl4溶液,振荡、静置后会发现下层液体的颜色为紫色,再将混合液倒入分液漏斗(填仪器名称)中,将两层液体分离.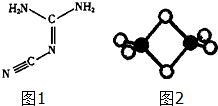 双氰胺结构简式如图1.
双氰胺结构简式如图1.