题目内容
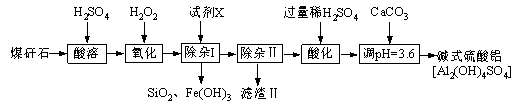
【题目】某地煤矸石经预处理后主要含SiO2(61%)、Al2O3(30%)和少量的Fe2O3、FeO及MgO。实验小组设计如下流程用其制备碱式硫酸铝[Al2(OH)4SO4]:
(1)为提高“酸浸”时铝浸出率,可采取的措施之一是 。
(2)氧化时应控制反应温度在10℃~20℃,其原因是 ,“氧化”时可用MnO2替代,发生的离子方程式 。
(3)试剂X为 ,设计一个简单的实验,证明铁元素已被沉淀完全: 。
(4)加入CaCO3制备碱式硫酸铝的化学方程式 。
【答案】(1)适当加热(或将煤矸石粉碎,适当提高硫酸的浓度等)
(2)防止H2O2分解 MnO2 + 2Fe2+ + 4H+ = Mn2+ + 2 Fe3+ + 2 H2O
(3)Al2O3;静置,取上层清液于试管中,滴加KSCN溶液,若溶液呈现血红色,说明未沉淀完全,反之则沉淀完全。
(4)Al2(SO4)3 + 2CaCO3 + 2H2O = Al2(OH)4SO4+2CaSO4+2CO2↑
【解析】
试题分析:煤矸石经预处理后主要含SiO2(61%)、Al2O3(30%)和少量的Fe2O3、FeO及MgO,由实验流程可知,加硫酸后,Al2O3、Fe2O3、FeO、MgO均与硫酸反应,只有SiO2不反应,酸溶后溶液中含Al3+、Fe2+、Fe3+、Mg2+,然后加过氧化氢氧化Fe2+,再加X为氧化铝、氢氧化铝等调节pH,促进铁离子水解转化为沉淀,则过滤得到滤渣为SiO2、Fe(OH)3,除杂II除去溶液中镁离子,滤渣Ⅱ为Mg(OH)2,然后滤液中加硫酸酸化,再加碳酸钙调节pH,从而制备Al2(OH)4SO4,
(1)为提高“酸浸”时铝浸出率,可采取的措施之一是适当加热(或将煤矸石粉碎,适当提高硫酸的浓度等)。
故答案为:适当加热(或将煤矸石粉碎,适当提高硫酸的浓度等);
(2)氧化时应控制反应温度在10℃~20℃,其原因是防止H2O2分解,“氧化”时可用MnO2替代,发生的离子方程式为MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O。
故答案为:防止H2O2分解;MnO2+2Fe2++4H+=Mn2++2Fe3++2H2O;
(3)试剂X为Al2O3,设计一个简单的实验,证明铁元素已被沉淀完全的方法为静置,取上层清液于试管中,滴加KSCN溶液,若溶液呈现血红色,说明未沉淀完全,反之则沉淀完全。
故答案为:Al2O3;静置,取上层清液于试管中,滴加KSCN溶液,若溶液呈现血红色,说明未沉淀完全,反之则沉淀完全;
(4)加入CaCO3制备碱式硫酸铝的化学方程式为Al2(SO4)3+2CaCO3+2H2O=Al2(OH)4SO4+2CaSO4+2CO2↑。
故答案为:Al2(SO4)3+2CaCO3+2H2O=Al2(OH)4SO4+2CaSO4+2CO2↑。

 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案【题目】甲、乙、丙、丁、戊的相互转化关系如图所示(反应条件略去,箭头表示一步转化)。下列各组物质中,满足如图所示转化关系的是

甲 | 乙 | 丙 | 戊 | |
A | Na2O2 | CO2 | O2 | Na |
B | Fe | H2O | Fe2O3 | H2 |
C | MgO | 盐酸 | MgCl2 | NaOH |
D | CuSO4 | Zn | Cu | 稀H2SO4 |