题目内容
下列有关说法不正确的是:
A.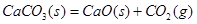 室温下不能自发进行,说明该反应的 室温下不能自发进行,说明该反应的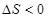 |
| B.镀铜铁制品镀层受损后,铁制品比受损前更容易生锈 |
C.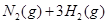  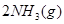 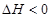 ,其他条件不变时升高温度,反应速率v(H2)和v(NH3)均增大 ,其他条件不变时升高温度,反应速率v(H2)和v(NH3)均增大 |
| D.水的离子积常数KW随着温度的升高而增大,说明水的电离是吸热过程 |
A
解析试题分析:A不正确,反应中有气体生成,熵值是增加的。室温下不能自发,是因为该反应是吸热反应;由于铁的金属性强于铜的,则镀铜铁制品镀层受损后,容易形成原电池,铁做负极,失去电子,即铁制品比受损前更容易生锈,B正确;其他条件不变时升高温度,正逆反应速率均是增大的,C正确;电离吸热,则升高温度,促进电离,所以电离常数增大,D正确,答案选A。
考点:考查反应自发性、金属腐蚀、外界条件对反应速率的影响、电离平衡常数的应用
点评:该题是高考中的常见题型,试题基础性强,贴近高考。意在培养学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和发散思维能力。

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
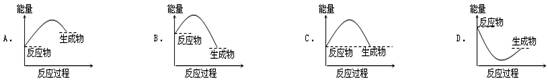
如图为某烯烃在催化剂作用下发生加成反应的能量变化图,下列有关叙述错误的是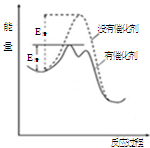
| A.催化剂能降低该反应的活化能 |
| B.催化剂能改变该反应的焓变 |
| C.该反应为放热反应 |
| D.由图可知,在催化剂作用下,该反应不是一步完成的 |
下列说法错误的是
| A.化学反应除了生成新的物质外,还伴随着能量的变化 |
| B.物质的燃烧一定是放热反应 |
| C.放热的化学反应不需要加热就能发生 |
| D.化学能与光能之间可以相互转化 |
下列反应中属吸热反应的是
| A.铝与盐酸反应放出氢气 | B.氢氧化钠与盐酸的反应 |
| C.硫在空气或氧气中燃烧 | D.Ba(OH)2·8H2O与NH4Cl反应 |
下列有关热化学方程式的叙述正确的是 ( )
| A.已知2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ/mol,则氢气的燃烧热为-285.8 kJ/mol |
| B.已知C(石墨,s)===C(金刚石,s) ΔH>0,则金刚石比石墨稳定 |
| C.含20.0 g NaOH的稀溶液与稀盐酸完全中和,放出28.7 kJ的热量,则稀醋酸和稀NaOH溶液反应的热化学方程式为:NaOH(aq)+CH3COOH(aq)===CH3COONa(aq)+H2O(l) ΔH=-57.4 kJ/mol |
| D.已知2C(s)+2O2(g)===2CO2(g) ΔH1;2C(s)+O2(g)===2CO(g) ΔH2,则ΔH1>ΔH2 |
(9分)(1)在25℃、101kPa下,1g甲烷燃烧生成CO2和液态水时放热55.6kJ。则表示甲烷燃烧热的热化学方程式为_________________________________________________。
(2)下表中的数据表示破坏1 mol化学键需消耗的能量(即键能,单位为kJ·mol-1):
| 化学键 | C—H | C—F | H—F | F—F |
| 键能 | 414 | 489 | 565 | 158 |
CH4(g)+4F2(g)= CF4(g)+4HF(g) △H=______________________。
(3) 下列说法正确的是(填序号)__ __:
A 相同温度下,0.1 mol?L-1NH4Cl溶液中NH4+的浓度比0.1 mol?L-1氨水中NH4+的浓度大;
B 用稀盐酸洗涤AgCl沉淀比用水洗涤损耗AgCl小;
C 电解饱和食盐水时,阳极得到氢氧化钠溶液和氢气;
D 对于Al(OH)3(s)
 Al(OH)3(aq)
Al(OH)3(aq) Al3+(aq)+3OH-(aq),前段为溶解平衡,后段是电离平衡;
Al3+(aq)+3OH-(aq),前段为溶解平衡,后段是电离平衡;E.除去溶液中的Mg2+,用OH-沉淀Mg2+比用CO32-效果好,说明Mg(OH)2的溶解度比MgCO3的大;