题目内容
18.一定量的饱和一元醇与足量的钠反应,可得到22.4L H2(标准状况下).等量的该醇完全燃烧生成264g CO2,该醇是( )| A. | 1丙醇 | B. | 乙醇 | C. | 1丁醇 | D. | 1戊醇 |
分析 根据n=$\frac{m}{M}$计算H2O、H2的物质的量,金属与醇反应,醇中-OH中的氢原子被还原生成氢气,根据H原子守恒可知,n(一元醇)=2n(H2),再求出1个醇分子中含有碳原子的个数,据此结合选项判断.
解答 解:醇和钠反应,生成氢气,实际反应的方程式是2ROH+2Na=2RONa+H2,22.4LH2的物质的量1mol,是根据方程式醇的物质的量就是1×2=2mol,264g CO2的物质的量是$\frac{264}{44}$=6mol,即1个醇分子中含有3个碳原子,且为饱和一元醇.
故选A.
点评 本题考查有机物分子式的确定,比较基础,判断氢气与一元醇的物质的量关系是关键.

练习册系列答案
相关题目
8.X、Y、Z、M、W五种短周期元素.X的质子总数与电子层数相同,Y、Z、M、W在周期表中的相对位置如表所示,且W原子核外电子数是M原子最外层电子数的2倍.
(1)五种元素原子半径从大到小排列为Si>N>O>F>H (均以元素符号表示,以下小题相同)
(2)写出W在周期表中的位置第三周期、IVA族,画出Z的离子结构示意图 .
.
(3)X、Y、Z 三种元素形成的化合物中属于离子化合物的物质的化学式是NH4NO3(或NH4NO2)
(4)W分别与M、Z元素形成的化合物WM4、WZ2分别属于分子 晶体、原子晶体,写出其中沸点较低的物质的电子式
(5)X分别与Y、Z、M、W形成的常见化合物中,稳定性最好的物质的结构式是H-F,稳定性最弱的物质的空间构型是正四面体,
(6)画出Y单质的电子式 .
.
(7)X的单质与Z的单质在KOH的溶液中可以形成原电池,已知A、B均为碳电极,在电池的A极通入X的单质气体,B极通入Z的单质气体,则B极的电极反应式为O2+2H2O+4e-=4OH-.
| Y | Z | M | |
| W |
(2)写出W在周期表中的位置第三周期、IVA族,画出Z的离子结构示意图
 .
.(3)X、Y、Z 三种元素形成的化合物中属于离子化合物的物质的化学式是NH4NO3(或NH4NO2)
(4)W分别与M、Z元素形成的化合物WM4、WZ2分别属于分子 晶体、原子晶体,写出其中沸点较低的物质的电子式

(5)X分别与Y、Z、M、W形成的常见化合物中,稳定性最好的物质的结构式是H-F,稳定性最弱的物质的空间构型是正四面体,
(6)画出Y单质的电子式
 .
.(7)X的单质与Z的单质在KOH的溶液中可以形成原电池,已知A、B均为碳电极,在电池的A极通入X的单质气体,B极通入Z的单质气体,则B极的电极反应式为O2+2H2O+4e-=4OH-.
9.质量比为2:3的铝分别与足量的盐酸和足量的氢氧化钠溶液反应,放出氢气在相同条件下的体积比为( )
| A. | 1:1 | B. | 1:2 | C. | 1:3 | D. | 2:3 |
6.下列说法正确的是( )
| A. | 分子式为C10H14的一元取代芳烃,其可能的结构有5种 | |
| B. | 分子式为C2H4O的只能表示一种物质 | |
| C. | 甲酸甲酯能发生银镜反应,并与丙酸互为同系物 | |
| D. | 丙烯在一定条件下与水反应主要产物是2-丙醇 |
13.已知H2(g)+Br2(g)=2HBr(g);△H=A KJ/mol,其它的相关数据如下表:
则表中a为( )
| H2(g) | Br2(g) | HBr(g) | |
| 1mol分子中的化学键断裂时需要吸收的能量/kJ | B | a | C |
| A. | A-B+C | B. | 2C-A-B | C. | C-A-B | D. | A-B+2C |
3.下列各组顺序的排列不正确的是( )
| A. | 金属性:Na<Mg<Al | B. | 热稳定性:HCl>H2S>PH3 | ||
| C. | 酸性强弱:H2CO3<HSO4<HClO4 | D. | 熔点:Na>K>Rb |
20.化学与生产、生活密切相关.下列叙述正确的是( )
| A. | 煤的干馏和煤的液化均是物理变化 | |
| B. | 海水淡化的方法有蒸馏法、电渗析法等 | |
| C. | 天然纤维和合成纤维的主要成分都是纤维素 | |
| D. | 用活性炭为糖浆脱色和用次氯酸盐漂白纸浆的原理相同 |
1.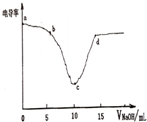 电导率可用于衡量电解质溶液的导电能力,即电导率越大,则溶液的导电能力越强.利用电导率传感器测得用0.100mol/L的NaOH溶液滴定10.00mL0.100mol/L的盐酸,电导率曲线如图所示.下列说法不正确的是( )
电导率可用于衡量电解质溶液的导电能力,即电导率越大,则溶液的导电能力越强.利用电导率传感器测得用0.100mol/L的NaOH溶液滴定10.00mL0.100mol/L的盐酸,电导率曲线如图所示.下列说法不正确的是( )
 电导率可用于衡量电解质溶液的导电能力,即电导率越大,则溶液的导电能力越强.利用电导率传感器测得用0.100mol/L的NaOH溶液滴定10.00mL0.100mol/L的盐酸,电导率曲线如图所示.下列说法不正确的是( )
电导率可用于衡量电解质溶液的导电能力,即电导率越大,则溶液的导电能力越强.利用电导率传感器测得用0.100mol/L的NaOH溶液滴定10.00mL0.100mol/L的盐酸,电导率曲线如图所示.下列说法不正确的是( )| A. | d点溶液中:c(Cl-)=2c(OH-)-2c(H+) | |
| B. | 电导率传感器能用于酸碱中和滴定终点的判断 | |
| C. | c点电导率最小是因为c点溶液的溶质为弱电解质 | |
| D. | c(Na+)、c(Cl-)对导电能力的影响比c(H+)、c(OH-)对导电能力的影响小 |
