题目内容
【题目】某研究小组向某2 L密闭容器中加入一定量的固体A和气体B,发生反应
A(s)+2B(g) ![]() D(g)+E(g) ΔH=Q kJ·mol-1。在T1 ℃时,反应进行到不同时间测得各物质的物质的量如表:
D(g)+E(g) ΔH=Q kJ·mol-1。在T1 ℃时,反应进行到不同时间测得各物质的物质的量如表:
时间(min) 物质的量(mol) | 0 | 10 | 20 | 30 | 40 | 50 |
B | 2.00 | 1.36 | 1.00 | 1.00 | 1.20 | 1.20 |
D | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
E | 0 | 0.32 | 0.50 | 0.50 | 0.60 | 0.60 |
(1)T 1 ℃时,该反应的平衡常数K=________。
(2)30 min后,只改变某一条件,反应重新达到平衡,根据表中的数据判断改变的条件可能是________(填字母编号)。
a.通入一定量的B
b.加入一定量的固体A
c.适当缩小容器的体积
d.升高反应体系温度
e.同时加入0.2 mol B、0.1 mol D、0.1 mol E
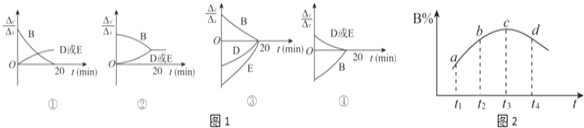
(3)对于该反应,用各物质表示的反应速率与时间的关系示意曲线为图1中的________(填序号)。
(4)维持容器的体积和温度T1 ℃不变,若向该容器中加入1.60 mol B、0.20 mol D、0.20 mol E和n mol A,达到平衡后,与表格中20分钟时各物质的浓度完全相同,则投入固体A的物质的量n的取值范围是________。
(5)维持容器的体积和温度T1 ℃不变,各物质的起始物质的量为:n(A)=1.0 mol,n(B)=3.0 mol,n(D)=a mol,n(E)=0 mol,达到平衡后,n(E)=0.50 mol,则a=________。
(6)若该密闭容器绝热,实验测得B的转化率B% 随温度变化的示意图如图2所示。由图可知,Q_______0(填“大于”或“小于”),c点v正_______v逆(填“大于”、“小于”或“等于”)。
【答案】0.25ae④大于0.3(或>0.3)1.5小于等于
【解析】
(1)平衡时生成物的浓度幂之积之反应物浓度的幂之积;(2)由图可知反应体系反应物和生成物的物质的量都增加;(3)依据化学反应达到平衡的过程分析和反应速率变化判断,达到平衡状态反应是可逆反应,正逆反应速率相同,速率之比等于化学方程式计量数之比;(4)由提供的数据可知,与表格中20分钟时各物质的浓度完全相同时,所以生成D、E的量为0.5-0.2=0.3mol,A的量要够转化所以A的量不小于0.3mol;(5)温度不变平衡常数不变,来求a的值;(6)最高点达平衡状态,温度升高B的转化率减小,所以正反应是放热反应。
(1)由表可知40分钟达平衡状态,结合平衡浓度和平衡常数概念计算,所以K=![]() =0.25;(2)30nim后,BDE都增加,由图可知反应体系反应物和生成物的物质的量都增加,可能增大反应物B的量,平衡正向移动,导致反应物和生成的物质的量都增加,或按变化量同时改变反应物和生成物,a.通入一定量的B平衡正向进行,BDE增大,故a符合;b.加入一定量的固体A不影响平衡移动,BDE不变,故b不符合;c.反应前后气体体积不变,适当缩小容器的体积,平衡不动,故c不符合;d.反应是吸热反应,升高反应体系温度,平衡正向进行,B减小,故d不符合;e.同时加入0.2molB、0.1molD、0.1molE,BDE浓度增大,故e符合;故选:ae;(3)A(s)+2B(g)
=0.25;(2)30nim后,BDE都增加,由图可知反应体系反应物和生成物的物质的量都增加,可能增大反应物B的量,平衡正向移动,导致反应物和生成的物质的量都增加,或按变化量同时改变反应物和生成物,a.通入一定量的B平衡正向进行,BDE增大,故a符合;b.加入一定量的固体A不影响平衡移动,BDE不变,故b不符合;c.反应前后气体体积不变,适当缩小容器的体积,平衡不动,故c不符合;d.反应是吸热反应,升高反应体系温度,平衡正向进行,B减小,故d不符合;e.同时加入0.2molB、0.1molD、0.1molE,BDE浓度增大,故e符合;故选:ae;(3)A(s)+2B(g)![]() D(g)+E(g)△H=QkJ/mol;反应前后气体体积不变;①B的反应速率不能为0;②B的反应速率和DE反应速率达到平衡状态不能相同;③DE变化速率 相同,图象不符;④DE速率相同,图象表示的是逆向进行,B反应速率增大,DE反应速率减小,故④正确;故答案为:④;(4)由提供的数据可知,与表格中20分钟时各物质的浓度完全相同时,所以生成D、E的量为0.5-0.2=0.3mol,A的量要够转化所以A的量不小于0.3mol,大于等于0.3mol;
D(g)+E(g)△H=QkJ/mol;反应前后气体体积不变;①B的反应速率不能为0;②B的反应速率和DE反应速率达到平衡状态不能相同;③DE变化速率 相同,图象不符;④DE速率相同,图象表示的是逆向进行,B反应速率增大,DE反应速率减小,故④正确;故答案为:④;(4)由提供的数据可知,与表格中20分钟时各物质的浓度完全相同时,所以生成D、E的量为0.5-0.2=0.3mol,A的量要够转化所以A的量不小于0.3mol,大于等于0.3mol;
(5) A(s)+2B(g)![]() D(g)+E(g)
D(g)+E(g)
起始量 3.0mol amol 0mol
平衡量 3-0.5×2 a+0.50 0.50mol
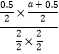 =0.25,解得a=1.5;(6)最高点达平衡状态,温度升高B的转化率减小,所以正反应是放热反应,即Q小于0,故答案为:小于;等于。
=0.25,解得a=1.5;(6)最高点达平衡状态,温度升高B的转化率减小,所以正反应是放热反应,即Q小于0,故答案为:小于;等于。

 春雨教育同步作文系列答案
春雨教育同步作文系列答案