题目内容
黄铁矿(主要成分为FeS2)是工业制取硫酸的重要原料,其燃烧产物为SO2和Fe2O3。
(1)已知1g FeS2完全燃烧放出7.1kJ热量,则表示FeS2完全燃烧反应的热化学方程式为:
______________________________________________________________。
(2)将0.050molSO2(g)和0.030molO2(g)放入容积为1L的密闭容器中,反应:2SO2(g)+O2(g)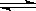 2SO3(g) 在一定条件下达到平衡,测得c(SO3)=0.040mol/L。则该条件下反应的平衡常数K的数值为___________,SO2的平衡转化率为__________。
2SO3(g) 在一定条件下达到平衡,测得c(SO3)=0.040mol/L。则该条件下反应的平衡常数K的数值为___________,SO2的平衡转化率为__________。
(3)当该反应处于平衡状态时,欲使平衡向正反应方向移动且反应速率加快,下列措施可行的是 。(填字母)
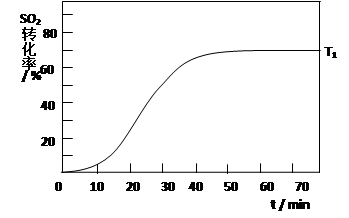
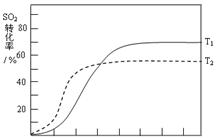
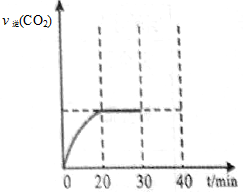
(4)反应:2SO2(g)+O2(g)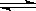 2SO3(g) △H<0 , SO2的转化率在起始温度T1=673K下随反应时间(t)的变化如下图,其他条件不变,仅改变起始温度为T2=723K,请在图中画出温度T2下SO2的转化率随反应时间变化的预期结果示意图。
2SO3(g) △H<0 , SO2的转化率在起始温度T1=673K下随反应时间(t)的变化如下图,其他条件不变,仅改变起始温度为T2=723K,请在图中画出温度T2下SO2的转化率随反应时间变化的预期结果示意图。
(1)已知1g FeS2完全燃烧放出7.1kJ热量,则表示FeS2完全燃烧反应的热化学方程式为:
______________________________________________________________。
(2)将0.050molSO2(g)和0.030molO2(g)放入容积为1L的密闭容器中,反应:2SO2(g)+O2(g)
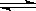 2SO3(g) 在一定条件下达到平衡,测得c(SO3)=0.040mol/L。则该条件下反应的平衡常数K的数值为___________,SO2的平衡转化率为__________。
2SO3(g) 在一定条件下达到平衡,测得c(SO3)=0.040mol/L。则该条件下反应的平衡常数K的数值为___________,SO2的平衡转化率为__________。(3)当该反应处于平衡状态时,欲使平衡向正反应方向移动且反应速率加快,下列措施可行的是 。(填字母)
| A.向平衡混合物中充入Ar | B.向平衡混合物中充入O2 |
| C.改变反应的催化剂 | D.降低反应的温度 |
 2SO3(g) △H<0 , SO2的转化率在起始温度T1=673K下随反应时间(t)的变化如下图,其他条件不变,仅改变起始温度为T2=723K,请在图中画出温度T2下SO2的转化率随反应时间变化的预期结果示意图。
2SO3(g) △H<0 , SO2的转化率在起始温度T1=673K下随反应时间(t)的变化如下图,其他条件不变,仅改变起始温度为T2=723K,请在图中画出温度T2下SO2的转化率随反应时间变化的预期结果示意图。
(1)4FeS2(s)+11O2(g) 2Fe2O3(s)+8SO2(g) △H=-3408kJ/mol (2分)
2Fe2O3(s)+8SO2(g) △H=-3408kJ/mol (2分)
(2)K=1.6×103(2分) 80% (2分) (3)B(1分,多选不得分)
 2Fe2O3(s)+8SO2(g) △H=-3408kJ/mol (2分)
2Fe2O3(s)+8SO2(g) △H=-3408kJ/mol (2分)(2)K=1.6×103(2分) 80% (2分) (3)B(1分,多选不得分)

试题分析:(1)FeS2完全燃烧燃烧的化学方程式是4FeS2+11O2
 2Fe2O3+8SO2,由于1g FeS2完全燃烧放出7.1kJ热量,则4molFeS2完全燃烧放出的热量是7.1kJ×120×4=3408kJ,所以该反应的热化学方程式是4FeS2(s)+11O2(g)
2Fe2O3+8SO2,由于1g FeS2完全燃烧放出7.1kJ热量,则4molFeS2完全燃烧放出的热量是7.1kJ×120×4=3408kJ,所以该反应的热化学方程式是4FeS2(s)+11O2(g) 2Fe2O3(s)+8SO2(g) △H=-3408kJ/mol。
2Fe2O3(s)+8SO2(g) △H=-3408kJ/mol。(2) 2SO2(g)+O2(g)
 2SO3(g)
2SO3(g)起始浓度(mol/L) 0.050 0.030 0
转化浓度(mol/L) 0.040 0.020 0.040
平衡浓度(mol/L) 0.010 0.010 0.040
所以该温度下平衡常数K=
 =1600
=1600SO2的平衡转化率=
 ×100%=80%
×100%=80%(3)向平衡混合物中充入Ar,容器容积不变,浓度不变,反应速率和平衡状态不变,A不正确;向平衡混合物中充入O2,增大反应物的浓度,反应速率增大,平衡向正反应方向移动,B正确;改变反应的催化剂平衡状态不变,C不正确;降低反应的温度,平衡向正反应方向移动,但反应速率降低,D不正确,答案选B。
(4)温度高反应速率快,到达平衡的时间减少。由于正反应是放热反应,所以温度高不利于平衡向正反应方向进行,SO2的转化率降低,因此正确的图像是
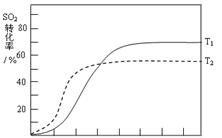 。
。点评:该题是高考中的常见考点和题型,属于中等难度试题的考查,试题综合性强,侧重对学生能力的培养和解题方法的指导与训练,旨在考查学生灵活运用基础知识解决实际问题的能力,有利于培养学生的逻辑推理能力和发散思维能力,提升学生的学科素养。

练习册系列答案
 暑假作业海燕出版社系列答案
暑假作业海燕出版社系列答案
相关题目
 2NH3(g) △H。下图I是合成氨反应的能量与反应过程相关图(未使用催化剂);图D是合成気反应在2L容器中、相同投料情况下、其它条件都不变时,某一反应条件的改变对反应的影响图。
2NH3(g) △H。下图I是合成氨反应的能量与反应过程相关图(未使用催化剂);图D是合成気反应在2L容器中、相同投料情况下、其它条件都不变时,某一反应条件的改变对反应的影响图。
 mol/(L·min)
mol/(L·min) 倍,则此温度下的平衡常数为_______。在同一温度,同一容器中,将起始物质改为amol N2 b molH2 c mol NH3 (a,b,c均不为零)欲使平衡混合物中各物质的质量与原平衡相同,则a,b,c满足的关系为_____________(用含a,b,c的表达式表示),且欲使反应在起始时向逆反应方向进行,c的取值范围是_______
倍,则此温度下的平衡常数为_______。在同一温度,同一容器中,将起始物质改为amol N2 b molH2 c mol NH3 (a,b,c均不为零)欲使平衡混合物中各物质的质量与原平衡相同,则a,b,c满足的关系为_____________(用含a,b,c的表达式表示),且欲使反应在起始时向逆反应方向进行,c的取值范围是_______ 2SO3(g) ?H=-196.6 kJ·mol-1
2SO3(g) ?H=-196.6 kJ·mol-1 2NO2(g) ?H=-113.0 kJ·mol-1
2NO2(g) ?H=-113.0 kJ·mol-1 

 CH3CH2OH(g) + H2O(g) △H =" —256.1" kJ·mol-1
CH3CH2OH(g) + H2O(g) △H =" —256.1" kJ·mol-1
 向
向 的转化,请你提出一条可行性建议 。
的转化,请你提出一条可行性建议 。 2CO2+N2。
2CO2+N2。 O2(g)=CO2(g) △H=-283.0kJ·mol-1
O2(g)=CO2(g) △H=-283.0kJ·mol-1 C(CO)/mol·L-1
C(CO)/mol·L-1
 2.70×10-3
2.70×10-3

 O2(g)=ZnO(s) △H =-351.1kJ·mol-1
O2(g)=ZnO(s) △H =-351.1kJ·mol-1 2NH3的能量变化如图所示,
2NH3的能量变化如图所示,
 N2(g)+
N2(g)+ H2(g)
H2(g)  =H2O(g) △H1=a kJ·
=H2O(g) △H1=a kJ·
 =2H2O(g) △H2=b kJ·
=2H2O(g) △H2=b kJ· =2H2O(l) △H4=d kJ·
=2H2O(l) △H4=d kJ·