题目内容
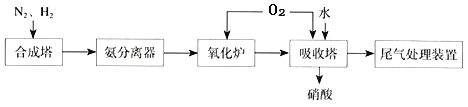
【题目】“低碳”在工业生产中意义重大,充分利用原材料,不排放或减少排放“三废”,不同工厂联合生产等都是很好的“低碳”生产方式。下面是几家工厂利用废气、废液、废渣联合生产化肥硫酸铵的工艺:
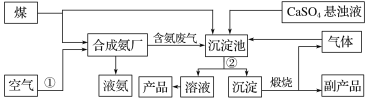
请回答下列问题:
(1)操作②为______________________________________________________。
(2)工业合成氨的化学方程式为_____________________。
(3)沉淀池中生成硫酸铵的化学方程式________________________________________。
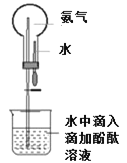
(4)在实验室中检验氨气的方法是_________________________________。
(5)副产品的化学式为________。该联合生产工艺中可以循环使用的物质是________。
【答案】过滤N2+3H2![]() 2NH3CaSO4+CO2+2NH3+H2O===CaCO3↓+(NH4)2SO4用湿润的红色石蕊试纸检验,若试纸变蓝,则说明含有NH3(或用玻璃棒蘸取浓盐酸检验,若产生白烟,则含有NH3)(其他合理答案均可)CaOCO2(若有NH3,均可)
2NH3CaSO4+CO2+2NH3+H2O===CaCO3↓+(NH4)2SO4用湿润的红色石蕊试纸检验,若试纸变蓝,则说明含有NH3(或用玻璃棒蘸取浓盐酸检验,若产生白烟,则含有NH3)(其他合理答案均可)CaOCO2(若有NH3,均可)
【解析】
煤和水蒸气反应生成氢气,利用空气中氮气和氢气在高温高压催化剂作用下反应生成氨气镁燃烧生成的二氧化碳、生成的氨气和硫酸钙仪器进入沉淀池中发生反应生成碳酸钙沉淀和产品,碳酸钙煅烧得到副产品氧化钙,生成的二氧化碳进入沉淀池循环使用。(1)操作②为分离固体与溶液;(2)工业合成氨是高温高压催化剂条件下反应生成氨气;(3)“产品”为(NH4)2SO4,反应物为CaSO4悬浊液、CO2、NH3等,产物除(NH4)2SO4外还有CaCO3,据此写出反应方程式;(4)通常用湿润的红色石蕊试纸检验NH3;(5)煅烧碳酸钙后可生成二氧化碳和氧化钙,氧化钙为副产品,二氧化碳可循环利用。
(1)将沉淀池中的混合物经过滤可得到产品和沉淀,则操作②为过滤;
(2)工业合成氨的化学方程式为:N2+3H2 ![]() 2NH3;
2NH3;
(3)“产品”是(NH4)2SO4,反应物是CaSO4悬浊液、CO2、NH3等,产物除(NH4)2SO4外还有CaCO3,其中离子方程中CaSO4悬浊液要写分子式,沉淀池中生成硫酸铵的化学方程式为:CaSO4+CO2+2NH3+H2O=CaCO3↓+(NH4)2SO4;
(4)利用湿润的红色石蕊试纸检验NH3,操作方法为:用湿润的红色石蕊试纸检验,若试纸变蓝,则说明含有NH3或用玻璃棒蘸取浓盐酸检验,若产生白烟,则含有NH3;
(5)CaCO3煅烧可生成CO2和CaO,其中CO2可循环使用,CaO为副产品。

 口算题卡北京妇女儿童出版社系列答案
口算题卡北京妇女儿童出版社系列答案【题目】Ⅰ、在2L密闭容器内,800℃时反应2NO(g)+O2(g)![]() 2NO2(g)体系中,n(NO)随时间的变化如下表:
2NO2(g)体系中,n(NO)随时间的变化如下表:
时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
n(NO)/mol | 0.020 | 0.010 | 0.008 | 0.007 | 0.007 | 0.007 |
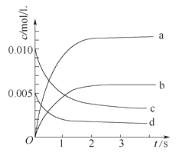
(1)下图中表示NO2的变化的曲线是_____。用NO表示从0~2 s内该反应的平均速率υ=_______。
(2)能说明该反应已达到平衡状态的是_______。
a.υ(NO2)=2υ(O2) b.容器内压强保持不变
c.υ逆(NO)=2υ正(O2) d.容器内密度保持不变
(3)下列措施能使该反应的速率增大是_______。
a.及时分离出NO2气体 b.适当升高温度
c.增大O2的浓度 d.选择高效催化剂