题目内容
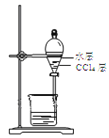
【题目】50mL0.5mol/L盐酸与50mL0.55mol/LNaOH溶液进行中和反应,通过测定反应过程中所放出的热量可计算中和热,下列说法正确的是
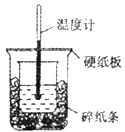
A.从实验装置上看,除了缺少环形玻璃搅拌棒外没有其他问题
B.大烧杯上如不盖硬纸板,测得的中和热数值会偏大
C.用相同浓度和体积的氨水代替NaOH溶液进行上述实验,测得中和热的数值会偏大
D.实验中改用60mL0.5mol/L盐酸跟50mL0.55mol/LNaOH溶液进行反应,与上实验相比,所放出的热量不相等,但是所求中和热相等
【答案】D
【解析】
A.从实验装置上看,缺少环形玻璃搅拌棒外,内外烧杯不一样高,热量损失大,A错误;
B.大烧杯上如不盖硬纸板,会导致热量损失大,使测得的中和热数值会偏小,B错误;
C.用相同浓度和体积的氨水代替NaOH溶液进行上述实验,由于NH3·H2O是弱电解质,电离吸收热量,使测得中和热的数值会偏小,C错误;
D.实验中改用60mL0.5mol/L盐酸跟50mL0.55mol/LNaOH溶液进行反应,与上实验相比,所放出的热量不相等,但是由于中和热是反应产生1mol水时所放出的热量,因此所求中和热相等,D正确;
故答案选D。

练习册系列答案
 应用题作业本系列答案
应用题作业本系列答案
相关题目
【题目】对于可逆反应N2(g)+3H2(g)![]() 2NH3(g) ΔH<0,下列研究目的和示意图相符的是( )
2NH3(g) ΔH<0,下列研究目的和示意图相符的是( )
A | B | C | D | |
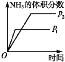
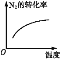
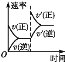
研究目的 | 压强对反应的影响(p2>p1) | 温度对反应的影响 | 平衡体系中增加N2的浓度对反应的影响 | 催化剂对反应的影响 |
示意图 |
|
|
|
|
A. AB. BC. CD. D