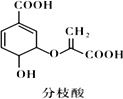
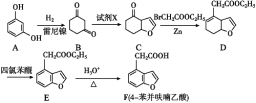
题目内容
【题目】下列离子方程式正确的是
A.用浓盐酸酸化的KMnO4溶液氧化H2C2O4:6H++5H2C2O4+2MnO4-=10CO2↑+2Mn2++8H2O
B.向Ca(HCO3)2溶液中滴加入少量NaOH溶液:Ca2++2HCO3-+2OH-=CaCO3↓+CO32-+2H2O
C.向Fe(NO3)3溶液中加入过量的HI溶液:2NO3-+8H++6I-=3I2+2NO↑+4H2O
D.用石墨电极电解MgCl2溶液:Mg2++2Cl-+2H2O![]() Mg(OH)2↓+H2↑+Cl2↑
Mg(OH)2↓+H2↑+Cl2↑
【答案】D
【解析】
A. 浓盐酸有还原性,也会与酸性高锰酸钾溶液发生反应: 2KMnO 4 +16HCl (浓) = 2KCl+ 2MnCl 2 + 5Cl 2 ↑+8H 2 O ,故不能证明草酸具有还原性,故A错误;
B. 向Ca(HCO3)2溶液中滴加入少量NaOH溶液,生成碳酸钙、碳酸氢钠和水,离子方程式:Ca2++HCO3-+OH-=CaCO3↓+H2O,故B错误;
C.硝酸铁溶液中滴加足量HI溶液,铁离子和硝酸根离子都参与反应,正确的离子方程式为: Fe3++3NO3-+12H++10I-=5I2+3NO↑+6H2O+ Fe2+,故C错误;
D. 石墨电极电解MgCl2溶液时,Cl-在阳极失电子生成氯气,水电离产生的H+在阴极得电子生成H2,同时Mg2+与OH-反应生成Mg(OH)2沉淀,离子方程式为Mg2++2Cl-+2H2O![]() Mg(OH)2↓+H2↑+Cl2↑,故D正确;
Mg(OH)2↓+H2↑+Cl2↑,故D正确;
故答案选D。

 阅读快车系列答案
阅读快车系列答案【题目】有机锌试剂(R—ZnBr)与酰氯(![]() )偶联可用于制备药物Ⅱ:
)偶联可用于制备药物Ⅱ:
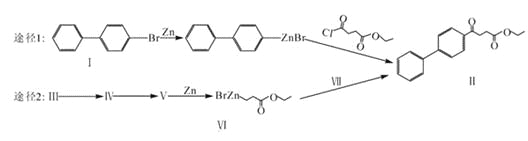
(1)化合物Ⅰ的分子式为_____________。
(2)关于化合物Ⅱ,下列说法正确的有______(双选)。
A.可以发生水解反应 |
B.可与新制的Cu(OH)2共热生成红色沉淀 |
C.可与FeCl3溶液反应显紫色 |
D.可与热的浓硝酸和浓硫酸混合液反应 |
(3)化合物Ⅲ含有3个碳原子,且可发生加聚反应,按照途径1合成线路的表示方式,完成途经2中由Ⅲ到Ⅴ的合成路线:_____________(标明反应试剂,忽略反应条件)。
(4)化合物Ⅴ的核磁共振氢谱中峰的组数为_____________,以H替代化合物Ⅵ中的ZnBr,所得化合物的羧酸类同分异构体共有_____________种(不考虑手性异构)。
(5)化合物Ⅵ和Ⅶ反应可直接得到Ⅱ,则化合物Ⅶ的结构简式为:_____________。
【题目】下图所示是元素周期表的部分轮廓图,根据元素①~⑩在周期表中的位置按题目要求回答:
① | |||||||||||||||||
② | ③ | ④ | |||||||||||||||
⑤ | ⑥ | ⑦ | ⑧ | ||||||||||||||
⑨ | |||||||||||||||||
⑩ |
(1)写出由元素①③④按原子个数比4:2:3组成的物质的化学式_______,其含有的化学键类型有________。
(2)元素⑤~⑧形成的简单离子中,离子半径由大到小的顺序为____________(用离子符号表示)。
(3)元素③⑦⑨的简单气态氢化物沸点由高到低的顺序排列是______(用化学式表示)。
(4)写出元素⑩的原子结构示意图______。
(5)元素②和④组成的一种化合物是引起温室效应的主要气体,其电子式为_________,将少量该化合物通入由元素④⑤⑥组成的一种盐溶液中,写出相应的化学方程式_____。
(6)元素⑧的一种氧化物通入氯化钡溶液无沉淀,通入硝酸钡溶液却会产生白色沉淀,写出少量该氧化物通入硝酸钡溶液的离子方程式___。