题目内容
 短周期主族元素A、B、C、D、E在元素周期表中的位置如下图所示:请回答下列问题:
短周期主族元素A、B、C、D、E在元素周期表中的位置如下图所示:请回答下列问题:(1)B、C、D元素电负性的大小顺序为:
O
O
>N
N
>C
C
(填元素符号).(2)E的氢化物与其最高价氧化物的水化物的钾盐共热能发生反应,生成一种气体单质,反应的化学方程式为
8HCl+KClO4═KCl+4Cl2↑+4H2O
8HCl+KClO4═KCl+4Cl2↑+4H2O
.(3)C有多种氧化物,其中甲的相对分子质量最小.在一定条件下,2L甲气体与0.5L氧气相混合,若该混合气体被足量的NaOH溶液完全吸收后没有气体残留,所生成的含氧酸盐的化学式
NaNO2
NaNO2
.(4)在298K下,A、B的单质各1mol完全燃烧,分别放出热量a kJ和b kJ.又知一定条件下,A的单质能将B从它的最高价氧化物中置换出来,若此置换反应生成3molB的单质,则该反应在298K下的△H=
-(4a-3b)KJ/mol
-(4a-3b)KJ/mol
(注:题中所设单质均为最稳定单质)(5)要证明与D同主族相邻元素F的非金属性与E的非金属性的强弱,正确、合理的实验操作及现象是
将氯水(或氯气)滴入(通入)到硫化钠(或硫化氢等)溶液中,有淡黄色沉淀生成
将氯水(或氯气)滴入(通入)到硫化钠(或硫化氢等)溶液中,有淡黄色沉淀生成
(6)用A、B的单质作电极,C的最高价氧化物的水化物稀溶液作电解质溶液构成原电池,写出此原电池正极的电极反应式
NO3-+3e-+4H+=NO↑+2H2O
NO3-+3e-+4H+=NO↑+2H2O
.(假设C只被还原至+2价)分析:根据元素周期表的结构,图示部分正好是元素周期表第二周期和第三周期的后半部分,故知A、B、C、D、E分别为:Al、C、N、O、Cl,
(1)同周期元素的原子,从左到右电负性越来越大;
(2)盐酸中的氯离子能够被强氧化剂高氯酸钾氧化为氯气;
(3)氮的氧化物中分子量最小的是NO,NO易被氧气氧化为NO2,能和氢氧化钠反应;
(4)分别得出A、B的单质各1mol完全燃烧的热化学方程式,根据盖斯定律确定A的单质将B从它的最高价氧化物中置换出来的焓变;
(5)非金属之间的置换反应可以确定非金属性的强弱;
(6)原电池的正极发生的是得电子的还原反应.
(1)同周期元素的原子,从左到右电负性越来越大;
(2)盐酸中的氯离子能够被强氧化剂高氯酸钾氧化为氯气;
(3)氮的氧化物中分子量最小的是NO,NO易被氧气氧化为NO2,能和氢氧化钠反应;
(4)分别得出A、B的单质各1mol完全燃烧的热化学方程式,根据盖斯定律确定A的单质将B从它的最高价氧化物中置换出来的焓变;
(5)非金属之间的置换反应可以确定非金属性的强弱;
(6)原电池的正极发生的是得电子的还原反应.
解答:解:根据元素周期表的结构,图示部分正好是元素周期表第二周期和第三周期的后半部分,故知A、B、C、D、E分别为:Al、C、N、O、Cl,
(1)同周期元素的原子,从左到右电负性越来越大,所以电负性:O>N>C,故答案为:O、N、C;
(2)盐酸中的氯离子能够被强氧化剂高氯酸钾氧化为氯气,方程式为:8HCl+KClO4═KCl+4Cl2↑+4H2O,故答案为:8HCl+KClO4═KCl+4Cl2↑+4H2O;
(3)氮的氧化物中分子量最小的是NO,在一定条件下,2LNO气体与0.5L氧气相混合,得到1L的NO2还剩余1LNO,等量的该混合气体被足量的NaOH溶液完全吸收后,所得溶液为亚硝酸钠,故答案为:NaNO2;
(4)在298K下,Al、C的单质各1mol完全燃烧,分别放出热量a kJ和b kJ,则热化学方程式为:①4Al(s)+3O2(g)═2Al2O3(s);△H=-4aKJ/mol;②C(s)+O2(g)═CO2(g);△H=-bKJ/mol,铝的单质能将碳从CO2中置换出来生成3molC的单质的方程式为:③4Al(s)+3CO2(g)═2Al2O3(s)+3C(s)的反应焓变=①-②×3=-(4a-3b)KJ/mol,故答案为:-(4a-3b)KJ/mol;
(5)非金属之间的置换反应可以确定非金属性的强弱,氯气的氧化性强于硫,故可以将氯气通到硫化钠溶液中置换出硫来证明,故答案为:将氯水(或氯气)滴入(通入)到硫化钠(或硫化氢等)溶液中,有淡黄色沉淀生成;
(6)用铝和石墨作电极,硝酸稀溶液作电解质溶液构成原电池,发生铝和硝酸之间的氧化还原反应,正极发生的是得电子的还原反应,故答案为:NO3-+3e-+4H+=NO↑+2H2O.
(1)同周期元素的原子,从左到右电负性越来越大,所以电负性:O>N>C,故答案为:O、N、C;
(2)盐酸中的氯离子能够被强氧化剂高氯酸钾氧化为氯气,方程式为:8HCl+KClO4═KCl+4Cl2↑+4H2O,故答案为:8HCl+KClO4═KCl+4Cl2↑+4H2O;
(3)氮的氧化物中分子量最小的是NO,在一定条件下,2LNO气体与0.5L氧气相混合,得到1L的NO2还剩余1LNO,等量的该混合气体被足量的NaOH溶液完全吸收后,所得溶液为亚硝酸钠,故答案为:NaNO2;
(4)在298K下,Al、C的单质各1mol完全燃烧,分别放出热量a kJ和b kJ,则热化学方程式为:①4Al(s)+3O2(g)═2Al2O3(s);△H=-4aKJ/mol;②C(s)+O2(g)═CO2(g);△H=-bKJ/mol,铝的单质能将碳从CO2中置换出来生成3molC的单质的方程式为:③4Al(s)+3CO2(g)═2Al2O3(s)+3C(s)的反应焓变=①-②×3=-(4a-3b)KJ/mol,故答案为:-(4a-3b)KJ/mol;
(5)非金属之间的置换反应可以确定非金属性的强弱,氯气的氧化性强于硫,故可以将氯气通到硫化钠溶液中置换出硫来证明,故答案为:将氯水(或氯气)滴入(通入)到硫化钠(或硫化氢等)溶液中,有淡黄色沉淀生成;
(6)用铝和石墨作电极,硝酸稀溶液作电解质溶液构成原电池,发生铝和硝酸之间的氧化还原反应,正极发生的是得电子的还原反应,故答案为:NO3-+3e-+4H+=NO↑+2H2O.
点评:本题是一道关于元素周期表的综合推断题,考查知识面广,难度较大.

练习册系列答案
相关题目
短周期主族元素A、B、C、D的原子序数依次增大.A、C原子序数相差8,A、B、C三种元素原子的最外层电子数之和为15,B原子最外层电子数等于A原子最外层电子数的一半.下列叙述正确的是( )
| A、原子半径:A<D<C<B | B、B、C、D分别与A形成的化合物一定含有相同的化学键 | C、最高价氧化物对应水化物的酸性:D<C | D、常温下,单质B能大量溶于浓硝酸中 |
短周期主族元素A、B、C的原子序数依次递增,A与C同主族,B原子的最外层电子数等于A原子的次外层电子数,它们原子的最外层电子数之和为10,则下列叙述正确的是( )
| A、原于半径A<B<C | B、A的气态氢化物稳定性大于C的气态氢化物稳定性 | C、A、C两元素最高价氧化物均可与水化合得到对应的酸 | D、高温时,A单质可以从C的氧化物中置换得到C单质 |
短周期主族元素A、B、C、D、E的原子序数依次增大,其中A与C同主族,A与其它元素不在同一周期,B与D同主族,常温下D的单质为淡黄色固体.下列推断中正确的是( )
| A、原子半径由小到大的顺序:r(C)<r(D)<r(E) | B、元素D、E分别与A形成的化合物的热稳定性:E>D | C、元素D的最高价氧化物对应水化物的酸性比E的强 | D、元素B分别与A、C形成的化合物中化学键的类型完全相同 |
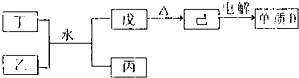
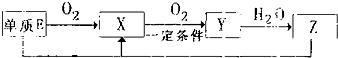
 短周期主族元素A、B、C、D、E的原子序数依次增大,它们原子核外的电子层数之和为10;B元素的化合物种类繁多,数目庞大.C、D两种元素形成的单质是空气中含量最多的物质;D、E两元素可以生成两种不同的离子化合物.
短周期主族元素A、B、C、D、E的原子序数依次增大,它们原子核外的电子层数之和为10;B元素的化合物种类繁多,数目庞大.C、D两种元素形成的单质是空气中含量最多的物质;D、E两元素可以生成两种不同的离子化合物. NH3?H2O+H+
NH3?H2O+H+ 2NO2
2NO2