题目内容
短周期主族元素A、B、C的原子序数依次递增,A与C同主族,B原子的最外层电子数等于A原子的次外层电子数,它们原子的最外层电子数之和为10,则下列叙述正确的是( )
| A、原于半径A<B<C | B、A的气态氢化物稳定性大于C的气态氢化物稳定性 | C、A、C两元素最高价氧化物均可与水化合得到对应的酸 | D、高温时,A单质可以从C的氧化物中置换得到C单质 |
分析:短周期主族元素A、B、C的原子序数依次递增,A与C同主族,它们原子的最外层电子数之和为10,则A、C不能处于ⅠA族,故A处于第二周期、C处于第三周期,B原子的最外层电子数等于A原子的次外层电子数,则B原子最外层电子数为2,A、C最外层电子数为
=4,则A为C原子、C为Si元素,B的原子序数介于C、Si之间,故B为Mg元素,据此解答.
| 10-2 |
| 2 |
解答:解:短周期主族元素A、B、C的原子序数依次递增,A与C同主族,它们原子的最外层电子数之和为10,则A、C不能处于ⅠA族,故A处于第二周期、C处于第三周期,B原子的最外层电子数等于A原子的次外层电子数,则B原子最外层电子数为2,A、C最外层电子数为
=4,则A为C原子、C为Si元素,B的原子序数介于C、Si之间,故B为Mg元素,
A.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径C<Si<Mg,故A错误;
B.非金属性C>Si,故C的气态氢化物稳定性大于Si的气态氢化物稳定性,故B正确;
C.二氧化硅不能与水化合生成硅酸,故C错误;
D.高温下,碳与二氧化硅反应生成硅与CO,用于工业生成硅,故D正确,
故选BD.
| 10-2 |
| 2 |
A.同周期自左而右原子半径减小,同主族自上而下原子半径增大,故原子半径C<Si<Mg,故A错误;
B.非金属性C>Si,故C的气态氢化物稳定性大于Si的气态氢化物稳定性,故B正确;
C.二氧化硅不能与水化合生成硅酸,故C错误;
D.高温下,碳与二氧化硅反应生成硅与CO,用于工业生成硅,故D正确,
故选BD.
点评:本题考查结构位置性质关系应用,推断元素是解题的关键,注意掌握元素周期律,注意短周期元素原子结构特点,充分利用最外层电子数进行推断.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
短周期主族元素A、B、C、D的原子序数依次增大.A、C原子序数相差8,A、B、C三种元素原子的最外层电子数之和为15,B原子最外层电子数等于A原子最外层电子数的一半.下列叙述正确的是( )
| A、原子半径:A<D<C<B | B、B、C、D分别与A形成的化合物一定含有相同的化学键 | C、最高价氧化物对应水化物的酸性:D<C | D、常温下,单质B能大量溶于浓硝酸中 |
短周期主族元素A、B、C、D、E的原子序数依次增大,其中A与C同主族,A与其它元素不在同一周期,B与D同主族,常温下D的单质为淡黄色固体.下列推断中正确的是( )
| A、原子半径由小到大的顺序:r(C)<r(D)<r(E) | B、元素D、E分别与A形成的化合物的热稳定性:E>D | C、元素D的最高价氧化物对应水化物的酸性比E的强 | D、元素B分别与A、C形成的化合物中化学键的类型完全相同 |
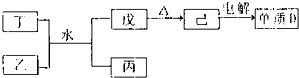
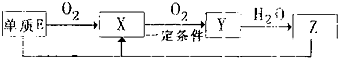
 短周期主族元素A、B、C、D、E的原子序数依次增大,它们原子核外的电子层数之和为10;B元素的化合物种类繁多,数目庞大.C、D两种元素形成的单质是空气中含量最多的物质;D、E两元素可以生成两种不同的离子化合物.
短周期主族元素A、B、C、D、E的原子序数依次增大,它们原子核外的电子层数之和为10;B元素的化合物种类繁多,数目庞大.C、D两种元素形成的单质是空气中含量最多的物质;D、E两元素可以生成两种不同的离子化合物. NH3?H2O+H+
NH3?H2O+H+ 2NO2
2NO2