题目内容
【题目】25℃时,将浓度均为0.1 mol·L-1、体积分别为Va和Vb的HX溶液与NH3·H2O溶液按不同体积比混合,保持Va+Vb=100mL,Va、Vb与混合液的pH的关系如图所示。下列说法不正确的是

A. Ka(HX)的值与Kb(NH3·H2O)的值相等
B. b点,c(NH4+)+c(HX)=0.05 mol·L-1
C. a→c点过程中, 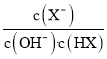 值不变
值不变
D. a、b、c三点,c点时水电离出的c(H+)最大
【答案】D
【解析】
A.b点加入等体积等浓度的HX和氨水,两者恰好完全反应生成NH4X,b点溶液的pH=7,说明X-与NH4+的水解程度相等,则Ka(HX)的值与Kb(NH3·H2O)的值相等,故A正确;
B.由图可知0.1 mol·L-1的HX溶液的pH=3,HX为弱酸,因为b点的pH=7,所以b点c(X-)=c(NH4+),,根据物料守恒c(X-)+c(HX)=0.1mol/L×0.05L/0.1L=0.05mol/L,则c(NH4+)+c(HX)=0.05 mol·L-1,故B正确;
C. a→ c点过程中,![]() ,水解平衡常数只与温度有关,温度不变,则
,水解平衡常数只与温度有关,温度不变,则![]() 值不变,故C正确;
值不变,故C正确;
D. b点加入等体积等浓度的HX和氨水,两者恰好完全反应生成NH4X,NH4X是弱酸弱碱盐,促进水电离,则a、b、c三点,b 点时水电离出的c(H+)最大,故D错误。答案选D。

练习册系列答案
 智慧课堂密卷100分单元过关检测系列答案
智慧课堂密卷100分单元过关检测系列答案
相关题目