题目内容
(10分)将CH4与H2O(g)通入聚焦太阳能反应器,发生反应:CH4(g)+H2O(g) CO(g)+3H2(g)
CO(g)+3H2(g)
(1)某温度下将等物质的量的CH4和H2O(g)充入密闭容器中,使容器体积为2L,控制容器体积不变,3min时反应达到平衡,平衡常数K=27,此时测得CO的物质的量为0.20mol,求①3min内H2的生成速率②CH4的平衡转化率(计算结果保留两位有效数字)。(需有计算过程)
(2)若和(1)相同的初始条件,但在恒压条件下进行该反应,则达平衡时,CH4的转化率与(1)的比较,是( )
 CO(g)+3H2(g)
CO(g)+3H2(g)(1)某温度下将等物质的量的CH4和H2O(g)充入密闭容器中,使容器体积为2L,控制容器体积不变,3min时反应达到平衡,平衡常数K=27,此时测得CO的物质的量为0.20mol,求①3min内H2的生成速率②CH4的平衡转化率(计算结果保留两位有效数字)。(需有计算过程)
(2)若和(1)相同的初始条件,但在恒压条件下进行该反应,则达平衡时,CH4的转化率与(1)的比较,是( )
| A.增大 | B.减小 | C.相等 | D.无法确定 |
(1)设CH4的物质的量浓度为xmol/L

(2)A

(2)A
(1)考查可逆反应的有关计算,已被采用三段式。
(2)由于反应是体积增大的可逆反应,所以反应(1)中的压强在反应过程中始终大于反应(2)。但压强大,平衡向逆反应方向移动,转化率降低,所以答案选A。
(2)由于反应是体积增大的可逆反应,所以反应(1)中的压强在反应过程中始终大于反应(2)。但压强大,平衡向逆反应方向移动,转化率降低,所以答案选A。

练习册系列答案
相关题目
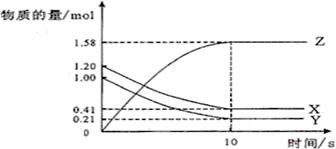
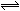 Z(g)
Z(g)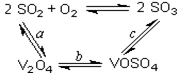
 SO3+ V2O4
SO3+ V2O4 
 2SO2+O2 在550 ℃时的平衡常数K= 。
2SO2+O2 在550 ℃时的平衡常数K= 。
 H++HA-,HA-
H++HA-,HA- pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则:
pC(g),达到平衡后,当升高温度时,B的转化率变大;当减小压强时,混合体系中C的质量分数也减小,则: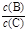 将_________。
将_________。 2NH3(g)△H<0,向某体积恒定的密闭容器中按体积比1﹕3充入N2和 H2,在一定条件下发生反应,下图是某物理量(Y)随时间(t)变化示意图,Y可以是( )
2NH3(g)△H<0,向某体积恒定的密闭容器中按体积比1﹕3充入N2和 H2,在一定条件下发生反应,下图是某物理量(Y)随时间(t)变化示意图,Y可以是( )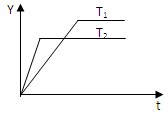
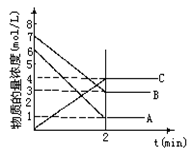
 4C
4C