��Ŀ����
��֪A��B��C��D��Ϊ������Ԫ�أ����ǵ�ԭ���������ε����� A�������Ϊһ�����ӵķǽ���Ԫ�أ�C ԭ�ӵ������������Ǵ�����3���� C��D���γ����ֹ�̬���������һ��Ϊ����ɫ���壻B��C���γɶ�����̬�����A��B��C����Ԫ�ؿ����γ����Ӿ��壬�þ����и�Ԫ��ԭ�ӵ����ʵ���֮��ΪA:B:C=4:2:3����ش��������⣺
(1)д��B��ԭ�ӽṹʾ��ͼ ��д��C��D�γɵĵ���ɫ���廯����ĵ���ʽ ��
(2)Ԫ��ԭ�ӵ����ʵ���֮��ΪA:B:C="4:" 2:3 �ľ�������Ϊ �� ��ˮ��Һ�� �ԣ��䷴Ӧ�����ӷ���ʽΪ ��
(3)��д��A2C��BA3�����е�������ͬ��������A��B��CԪ������������Ԫ����ɵ����ķ��ţ��������� �� ��
(4)д����B��CԪ�������Ԫ��ԭ��������ΪB:C=7:12�Ļ�����Ļ�ѧʽ ��
(1)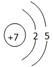 (2) ����泥��NH4++H2O
(2) ����泥��NH4++H2O  NH3��H2O + H+
NH3��H2O + H+
(3) NH4+, NH2�C,OH�C, H3O+�� ��4��N2O3
�������������A�������Ϊһ�����ӵķǽ���Ԫ�أ���A����Ԫ�أ�C ԭ�ӵ������������Ǵ�����3��������C����Ԫ�أ� C��D���γ����ֹ�̬���������һ��Ϊ����ɫ���壬��DӦ������Ԫ�أ�B��C���γɶ�����̬�����A��B��C����Ԫ�ؿ����γ����Ӿ��壬�þ����и�Ԫ��ԭ�ӵ����ʵ���֮��ΪA:B:C��4:2:3����B��ԭ������С����Ԫ�صģ�����B�ǵ�Ԫ�ء�
��1����ԭ�ӵ�ԭ�ӽṹʾ��ͼ�� ���������Ƶĵ���ʽ��
���������Ƶĵ���ʽ�� ��
��
��2���þ���������泥�����ˮˮ����Һ�����ԣ����ӷ���ʽ��NH4++H2O  NH3��H2O + H+��
NH3��H2O + H+��
��3��ˮ�Ͱ�����10��������������A��B��CԪ������������Ԫ����ɵ����ķ�����NH4+, NH2�C,OH�C, H3O+�ȡ�
��4����B��CԪ�������Ԫ��ԭ��������ΪB:C��7:12��������ԭ�ӵĸ���֮����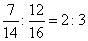 �����û�������N2O3��
�����û�������N2O3��
���㣺����Ԫ�����ڱ��Ľṹ�Լ�Ԫ�������ɵ�Ӧ�ú��ж�
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣���������ǿ�����ض�ѧ������֪ʶ�Ĺ��̺�ѵ�������������ѧ����������������Ӧ��������������Ҫ��Ԫ�ء�λ�������ԡ����߹�ϵ���ۺϿ��飬�Ƚ�ȫ�濼��ѧ���й�Ԫ���ƶ�֪ʶ���������֪ʶ�������������ԡ����ڱ���Ԫ�ص��ƶϡ�Ϊ���壬����ѧ����Ԫ�����ڱ�����Ϥ�̶ȼ���Ա��и�Ԫ�����ʺ���Ӧԭ�ӽṹ�������Եݱ���ɵ���ʶ�����ճ̶ȡ�������ѧ�������ʽṹ�����ʹ�ϵ�Լ�����Ԫ�������ɽ�����廯ѧ�����������

 �Űٷֿ�ʱ����ϵ�д�
�Űٷֿ�ʱ����ϵ�д� ������״Ԫ��ҵϵ�д�
������״Ԫ��ҵϵ�д� ��ʱ�ƿ�������ϰϵ�д�
��ʱ�ƿ�������ϰϵ�д�



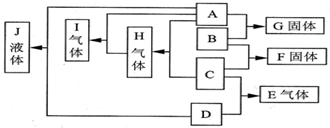

 ��֪A��B��C��D��Ϊ���壬E��F��Ϊ�����³ʹ�������ӻ����GΪ�Ȼ��ƣ�A��B��ȼ�յĻ���ʲ�ɫ����Ӧ���������������д������̣�����֮���ת����ϵ��ͼ��ʾ��
��֪A��B��C��D��Ϊ���壬E��F��Ϊ�����³ʹ�������ӻ����GΪ�Ȼ��ƣ�A��B��ȼ�յĻ���ʲ�ɫ����Ӧ���������������д������̣�����֮���ת����ϵ��ͼ��ʾ��


