题目内容
已知A、B、C、D均为气体,其中气体A、B为单质且A气体常温下呈黄绿色,A在B中燃烧的火焰呈苍白色,D气体的水溶液呈碱性,F溶液俗称石灰水,反应②中两气体相遇有大量白烟,G为氯化钙,它们之间的转化关系如图所示:

(1)写出A、B、D的化学式:A
(2)D气体水溶液的电离方程式:
(3)在反应①~③中,属于氧化还原反应的是
(4)反应②的化学方程式为:

(1)写出A、B、D的化学式:A
Cl2
Cl2
,BH2
H2
,DNH3
NH3
.化合物D、H均含10电子,写出同含10电子的阳离子化学式NH4+、H3O+
NH4+、H3O+
.(2)D气体水溶液的电离方程式:
NH3.H2O?NH4++OH-
NH3.H2O?NH4++OH-
;E的水解反应离子方程式:NH4++H2O?NH3.H2O+H+
NH4++H2O?NH3.H2O+H+
.(3)在反应①~③中,属于氧化还原反应的是
①
①
.(4)反应②的化学方程式为:
HCl+NH3═NH4Cl
HCl+NH3═NH4Cl
;反应③的化学方程式为:Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O
| ||
Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O
.
| ||
分析:A气体常温下呈黄绿色,则A为Cl2,A在B中燃烧的火焰呈苍白色,B为H2,C为HCl,D气体的水溶液呈碱性,则D为NH3,所以E为NH4Cl,F溶液俗称石灰水,则F为Ca(OH)2,G为氯化钙,则H为水,然后结合元素化合物性质及化学用语来解答.
解答:解:A气体常温下呈黄绿色,则A为Cl2,A在B中燃烧的火焰呈苍白色,B为H2,C为HCl,D气体的水溶液呈碱性,则D为NH3,所以E为NH4Cl,F溶液俗称石灰水,则F为Ca(OH)2,G为氯化钙,则H为水,
(1)由上述分析可知,A为Cl2,B为H2,D为NH3,同含10电子的阳离子化学式分别为NH4+、H3O+,故答案为:Cl2;H2;NH3;NH4+、H3O+;
(2)D气体水溶液的电离方程式为NH3.H2O?NH4++OH-,E的水解反应离子方程式为NH4++H2O?NH3.H2O+H+,
故答案为:NH3.H2O?NH4++OH-;NH4++H2O?NH3.H2O+H+;
(3)反应①为Cl2+H2═2HCl,反应②为HCl+NH3═NH4Cl,反应③为Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O,只有反应①中有元素化合价变化,属于氧化还原反应,
故答案为:①;
(4)反应②为HCl+NH3═NH4Cl,反应③为Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O,故答案为:HCl+NH3═NH4Cl;Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O.
(1)由上述分析可知,A为Cl2,B为H2,D为NH3,同含10电子的阳离子化学式分别为NH4+、H3O+,故答案为:Cl2;H2;NH3;NH4+、H3O+;
(2)D气体水溶液的电离方程式为NH3.H2O?NH4++OH-,E的水解反应离子方程式为NH4++H2O?NH3.H2O+H+,
故答案为:NH3.H2O?NH4++OH-;NH4++H2O?NH3.H2O+H+;
(3)反应①为Cl2+H2═2HCl,反应②为HCl+NH3═NH4Cl,反应③为Ca(OH)2+2NH4Cl
| ||
故答案为:①;
(4)反应②为HCl+NH3═NH4Cl,反应③为Ca(OH)2+2NH4Cl
| ||
| ||
点评:本题考查无机物的推断,注意利用信息推断各物质是解答的关键,明确氯气的性质及氨气的制法即可解答,颜色为解答的突破口,题目难度中等.

练习册系列答案
相关题目




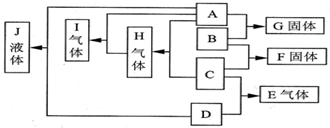

 已知A、B、C、D均为气体,E、F均为常温下呈固体的离子化合物,G为氯化钙,A在B中燃烧的火焰呈苍白色,反应②中两气体相遇有大量白烟,它们之间的转化关系如图所示:
已知A、B、C、D均为气体,E、F均为常温下呈固体的离子化合物,G为氯化钙,A在B中燃烧的火焰呈苍白色,反应②中两气体相遇有大量白烟,它们之间的转化关系如图所示:

