题目内容
17.从樟科植物枝叶提取的精油中含有下列甲、乙、丙三种成分: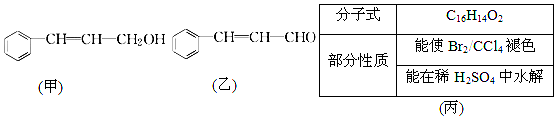
(1)甲中除苯环外,官能团的名称为羟基和碳碳双键.
(2)由甲转化为乙需经下列过程(已略去各步反应的无关产物,下同):
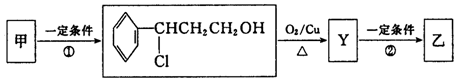
则Ⅰ的反应类型为加成反应,Ⅱ的化学方程式为
 +NaOH$→_{△}^{醇}$
+NaOH$→_{△}^{醇}$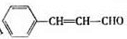 +NaCl+H2O(注明反应条件).
+NaCl+H2O(注明反应条件).(3)已知:
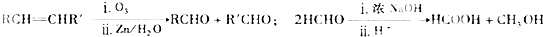
由乙制丙的一种合成路线图如下(A~F均为有机物,图中Mr表示相对分子质量):
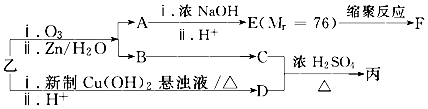
①下列物质不能与C反应的是c(选填序号)
a.金属钠 b.HBr c.Na2CO3溶液 d.乙酸
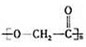
②写出F的结构简式
 .
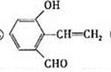
.③D有多种同分异构体,任写其中一种能同时满足下列条件的异构体结构简式
 .
.a.苯环上连接着三种不同官能团 b.能发生银镜反应
c.能与Br2/CCl4发生加成反应 d.遇FeCl3溶液显示特征颜色
④综上分析,丙的结构简式为
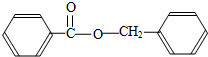 .
.
分析 (1)根据甲的结构简式及官能团的概念来回答;
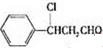
(2)根据甲发生转化时结构上的变化可知,甲与氯化氢发生加成反应得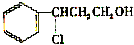 ,
,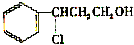 发生氧化得Y为
发生氧化得Y为 ,Y发生消去反应得乙;
,Y发生消去反应得乙;
(3)根据乙的结构简式和题干中所给信息,可知A是乙二醛,B是苯甲醛,所以D是苯甲酸,苯甲醛易被还原为苯甲醇,苯甲醇和苯甲酸之间能发生酯化反应,所以C是苯甲醇,属于醇类,能和金属钠反应、能和氢卤酸反应、能和酸之间发生酯化反应,根据题意信息,A发生信息中的反应得E,E是相对分子质量为76,则E为OH-CH2-COOH,本身能发生缩聚反应生成 ,据此答题.
,据此答题.
解答 解:(1)根据甲的结构简式可知,甲中含有官能团是羟基和碳碳双键,
故答案为:羟基和碳碳双键;
(2)经过反应Ⅰ发现碳碳双键成为了单键,并且引入了Cl原子,所以反应为甲和氯化氢之间发生了加成反应,含有醇羟基的物质,如果邻位碳上有氢原子,则被氧化为醛基,氯代烃中如果含有邻位氢原子则会发生消去反应,所以Ⅱ的方程式为: +NaOH$→_{△}^{醇}$
+NaOH$→_{△}^{醇}$ +NaCl+H2O,
+NaCl+H2O,
故答案为:加成反应; +NaOH$→_{△}^{醇}$
+NaOH$→_{△}^{醇}$ +NaCl+H2O;
+NaCl+H2O;
(3)根据乙的结构简式和题干中所给信息,可知A是乙二醛,B是苯甲醛,所以D是苯甲酸,苯甲醛易被还原为苯甲醇,苯甲醇和苯甲酸之间能发生酯化反应,所以C是苯甲醇,属于醇类,能和金属钠反应、能和氢卤酸反应、能和酸之间发生酯化反应,根据题意信息,A发生信息中的反应得E,E是相对分子质量为76,则E为OH-CH2-COOH,本身能发生缩聚反应生成 ,
,
①C是苯甲醇,属于醇类,能和金属钠反应、能和氢卤酸反应、能和酸之间发生酯化反应,Na2CO3溶液不能与C反应,
故答案为:c;
②OH-CH2-COOH本身能发生缩聚反应生成 ,F的结构简式为:
,F的结构简式为: ,
,
故答案为: .
.
③D的同分异构体,能发生银镜反应,则含有醛基,能与Br2/CCl4发生加成反应,则含有不饱和键,遇FeCl3溶液显示特征颜色,则含有酚羟基,能同时满足各个条件的异构体结构简式为: ,
,
故答案为: ;
;
④综上分析,D是苯甲酸,C是苯甲醇,二者之间可以发生酯化反应得到苯甲酸苯甲酯,所以丙的结构简式为 ,
,
故答案为: .
.
点评 该题考查有机物的推断,是高考中的常见题型,属于中等难度的试题,试题基础性强,侧重对学生能力的培养和解题方法的指导与训练,有助于培养学生的逻辑推理能力和发散思维能力.该题的关键是明确各种官能团结构和性质,然后结合题意具体问题、具体分析即可,有助于培养学生的创新思维能力和应试能力.

 智能训练练测考系列答案
智能训练练测考系列答案| A. | 需要加热才能发生的反应可能是吸热反应也可能是放热反应 | |
| B. | 1 mol强酸与1mol强碱发生中和反应所放出的热量叫做中和热 | |
| C. | 二次电池充电时将电能转化为化学能 | |
| D. | 催化剂表面做成蜂窝状更有利于提高催化效果 |

(1)提出合理假设
假设1:该白色粉末成分为碳酸钠;
假设2:该白色粉末成分为亚硫酸钠;
假设3:该白色粉末成分为碳酸钠和亚硫酸钠的混合物.
(2)从上述仪器和试剂中选择合适的组合,一次性判断出该白色粉末的组成,其最佳连接顺序是:a-f-g-b-c-d-e(每组选用仪器和试剂限用一次).
(3)根据(2)的连接顺序进行实验,填写相应现象.
| 假设方案编号 | 相应现象 |
| 假设1 | 品红试液不褪色,澄清石灰水变浑浊 |
| 假设2 | 品红试液褪色,澄清石灰水不变浑浊 |
| 假设3 | 品红试液褪色,酸性高锰酸钾溶液颜色变浅(或不褪色),澄清石灰水变浑浊 |
| A. | 1molH2O的质量是18g/mol | |
| B. | CH4的摩尔质量是16g | |
| C. | 3.01×1023个CO2分子的质量是22g | |
| D. | 标准状况下,1mol任何物质的体积均为22.4L |
H2O2+I-→H2O+IO-
H2O2+IO-→H2O+O2+I-.
下列有关该反应的说法不正确的是( )
| A. | H2O2(l)═2H2O(g)+O2(g)△H=-196kJ•mol-1 | |
| B. | 在该反应中H2O2既做氧化剂.又做还原剂 | |
| C. | 反应速率与I-浓度有关 | |
| D. | v(H2O2)=v(H2O)=v(O2) |
 今有碱金属的两种碳酸盐和碱土金属(第二主族)的一种不溶性碳酸盐组成的混合物,取其7.560g与过量盐酸完全反应,放出CO2体积为1.344L(标况下)另取等质量的原混合物,加水搅拌,可滤出不溶性盐1.420g.
今有碱金属的两种碳酸盐和碱土金属(第二主族)的一种不溶性碳酸盐组成的混合物,取其7.560g与过量盐酸完全反应,放出CO2体积为1.344L(标况下)另取等质量的原混合物,加水搅拌,可滤出不溶性盐1.420g.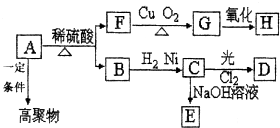 某高聚物的单体A(C11H12O2)可发生如图变化:
某高聚物的单体A(C11H12O2)可发生如图变化: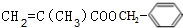 $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$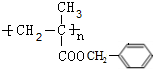 .
.
 ,含有离子键和共价键(填化学键类型),属于离子化合物 (填“离子化合物”或“共价化合物”)
,含有离子键和共价键(填化学键类型),属于离子化合物 (填“离子化合物”或“共价化合物”)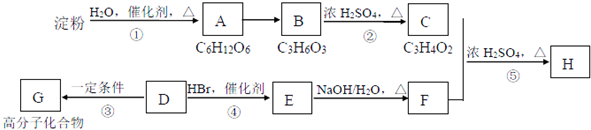
 ;反应类型:加聚反应.反应④的化学方程式:CH3CH=CH2+HBr$\stackrel{催化剂}{→}$CH3CHBrCH3;反应类型:加成反应.
;反应类型:加聚反应.反应④的化学方程式:CH3CH=CH2+HBr$\stackrel{催化剂}{→}$CH3CHBrCH3;反应类型:加成反应.