题目内容
99 ℃时,KW=1×10-12 mol2·L-2,在该温度下,将100 mL 0.001 mol·L-1的氢氧化钠溶液加水稀释至1 L,则溶液的pH为_______。若加水稀释至1 000 L,则溶液的pH近似为_______。
解析:稀释后,[OH-]=[NaOH]=![]() =1×10-4 mol·L-1,
=1×10-4 mol·L-1,
[H+]=![]() ,pH=8,若加水稀释至1 000 L,由碱电离出的[OH-]碱=
,pH=8,若加水稀释至1 000 L,由碱电离出的[OH-]碱=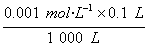 =1×10-7 mol·L-1,小于纯水电离出的[OH-]=1×10-6 mol·L-1,故溶液中[OH-]主要由水电离决定。[OH-]≈1×10-6 mol·L-1,pH=6。?
=1×10-7 mol·L-1,小于纯水电离出的[OH-]=1×10-6 mol·L-1,故溶液中[OH-]主要由水电离决定。[OH-]≈1×10-6 mol·L-1,pH=6。?
答案:8 6

练习册系列答案
相关题目