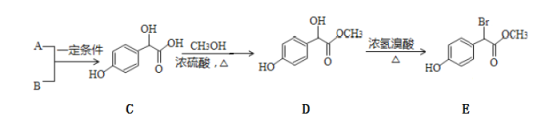
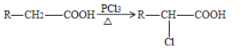题目内容
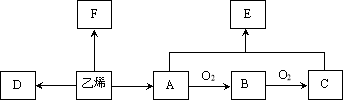
【题目】异丙苯(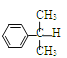 )氧化法是工业生产苯酚和丙酮最主要的方法。其反应和流程如下:
)氧化法是工业生产苯酚和丙酮最主要的方法。其反应和流程如下:
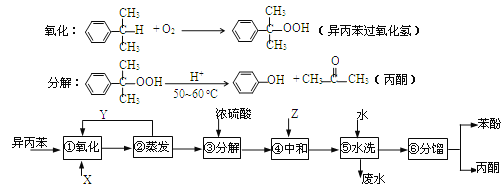
已知:
完成下列填空:
(1).X物质是 ;Y物质是 。
(2).浓硫酸的作用是 ,其优点是用量少,可能的缺点是 (写一条)。
(3).Z物质最适宜选择 (选填编号)。
a.NaOH b.Na2CO3c.NaHCO3d.CaCO3
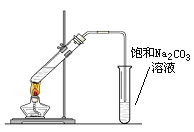
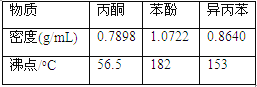
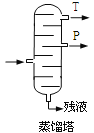
(4).步骤⑥分馏,工业上在分馏塔中进行,如右图,产品T是 ,请说明理由 。
废水中苯酚的含量,可根据苯酚与溴水的反应,用以下方法测定:
①把20.00mL废水、20mLKBrO3和KBr混合溶液[其中:
c(KBrO3)=0.0100mol/L,c(KBr)=0.0600mol/L]置于锥形瓶中,再加入10mL6mol/L的盐酸,迅速盖好盖子,摇动锥形瓶。
②充分反应后,稍松开瓶塞,从瓶塞和瓶壁间缝隙迅速加入10%KI溶液10mL(过量),迅速加盖,充分摇匀。加入少许淀粉溶液。
③用0.0250 mol/LNa2S2O3标准溶液滴定至终点。用去Na2S2O3溶液22.48mL。
(5).已知:BrO3–+5Br–+6H+→3Br2 + 3H2O ;写出苯酚与浓溴水反应的化学方程式 ;
第①步加盐酸、第②步加KI溶液,要迅速盖好盖子的原因是 。
(6).已知:I2+ 2Na2S2O3→2NaI + Na2S4O6;滴定终点的现象是 ;该废水中苯酚的浓度是 mol/L(保留4位小数)。
【答案】(1).氧气(或空气);异丙苯
(2).催化剂(1分),浓硫酸会使有机物发生脱水等副反应(浓硫酸与有机物混合放出大量热,使反应温度过高,不利于反应进行;或浓硫酸会腐蚀设备等),合理即得分) (3).c
(4).丙酮(1分) 丙酮的沸点低
(5).![]() ,防止溴挥发
,防止溴挥发
(6).由蓝色变为无色(或白色浑浊)且半分钟内不变色 0.0053
【解析】试题(1).在反应器A发生信息中的反应①,故需要氧气或空气,Y为未反应的异丙苯,循环利用。
(2).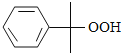 在浓硫酸作条件下分解得到
在浓硫酸作条件下分解得到![]() 、
、![]() ,浓硫酸作作催化剂,浓硫酸腐蚀性强,容易腐蚀设备;
,浓硫酸作作催化剂,浓硫酸腐蚀性强,容易腐蚀设备;
(3).加入Z的目的是中和硫酸,且不能与苯酚反应,a.NaOH能与硫酸、苯酚反应,故不选;b.CaCO3为固体,且与硫酸反应生成的硫酸钙微溶,会阻止碳酸钙与硫酸的反应,故b不选;c.NaHCO3能与硫酸反应,不与苯酚反应,故c选;d.CaO能与苯酚反应,且与硫酸反应生成的硫酸钙微溶,会阻止碳酸钙与硫酸的反应,故d不选;故选c;(4).由于丙酮的沸点低于苯酚,沸点越低越先蒸出,处于蒸馏塔的上部,则T为丙酮;理由为丙酮的沸点低于苯酚;(5).写出苯酚与浓溴水反应的化学方程式![]() ;溴易挥发,可防挥发;(6).滴定终点的现象是由蓝色变为无色(或白色浑浊)且半分钟内不变色; 20mLKBrO3和KBr混合溶液c(KBrO3)=0.0100mol/L,c(KBr)=0.0600mol/L在盐酸酸化的条件下可生成Br2的物质的量为0.0100mol/L×0.02L×3=0.0006mol,根据I2+ 2Na2S2O3→2NaI + Na2S4O6反应可Br2氧化KI得到的I2的物质的量为0.0250 mol/L×0.02248L×1/2=0.000281mol,结合Br2+2I-=I2+2Br-,可知与苯酚反应的Br2的物质的量为0.0006mol-0.000281mol=0.000319mol,可知苯酚的物质的量为0.000319mol×1/3=0.000106mol,则苯酚的浓度为0.000106mol÷0.020L=0.0053mol/L。
;溴易挥发,可防挥发;(6).滴定终点的现象是由蓝色变为无色(或白色浑浊)且半分钟内不变色; 20mLKBrO3和KBr混合溶液c(KBrO3)=0.0100mol/L,c(KBr)=0.0600mol/L在盐酸酸化的条件下可生成Br2的物质的量为0.0100mol/L×0.02L×3=0.0006mol,根据I2+ 2Na2S2O3→2NaI + Na2S4O6反应可Br2氧化KI得到的I2的物质的量为0.0250 mol/L×0.02248L×1/2=0.000281mol,结合Br2+2I-=I2+2Br-,可知与苯酚反应的Br2的物质的量为0.0006mol-0.000281mol=0.000319mol,可知苯酚的物质的量为0.000319mol×1/3=0.000106mol,则苯酚的浓度为0.000106mol÷0.020L=0.0053mol/L。