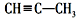题目内容
5.某化学兴趣小组对加碘食盐中碘酸钾进行研究,查阅资料得知:碘酸钾是一种白色粉末,常温下很稳定,加热至560℃开始分解.在酸性条件下碘酸钾是一种较强的氧化剂,与氢碘酸、过氧化氢等物质作用,被还原为单质碘.(1)学生甲设计实验测出加碘食盐中碘元素的含量,步骤如下:
a.称取14.1g加碘盐,加适量蒸馏水溶解;
b.用稀硫酸酸化,再加入过量KI溶液;
c.以淀粉为指示剂,用物质的量浓度为1.00×10-3mol•L-1的Na2S2O3溶液滴定(滴定时的反应方程式:I2+2S2O32-=2I-+S4O62-)滴定至终点时消耗20.OOmL.
①实验前,首先要精确配制1.00×10-3mol•L-1Na2S2O3溶液250mL,配制时需要的仪器除电子天平、玻璃棒、烧杯、胶头滴管外,还需250mL容量瓶.
②滴定到终点时,溶液由蓝色为无色,且半分钟内未恢复.加碘食盐样品中的碘元素含量是30.0mg/kg(结果保留一位小数).
(2)学生乙对纯净的NaCl(不含KIO3)进行了下列实验:
| 实验步骤 | 实验操作 | 实验现象 |
| ① | 取少量纯净的NaCl,加蒸馏水溶解 | 溶液无变化 |
| ② | 滴入淀粉KI溶液,振荡; | 溶液无变化 |
| ③ | 然后再滴加稀硫酸,振荡. | 溶液变蓝色 |
(3)工业上通常用电解KI溶液的方法来制备碘酸钾,电解过程中请你帮助学生丙设计实验来判断电解是否完全.仪器不限,可选的试剂:淀粉溶液、H2O2溶液、稀硫酸.
| 实验实验操作 | 实验实验现象及结论 |
分析 (1)①依据盐类水解分析判断,Na2S2O3为强碱弱酸盐,精确配制1.00×10-3mol•L-1Na2S2O3溶液250mL需要在250ml容量瓶中配制,结合溶液配制的实验过程分析需要的仪器;
②碘单质遇淀粉显蓝色,当碘单质消耗,蓝色褪去;根据反应找出反应关系式,然后根据题中数据计算出加碘食盐样品中的碘元素含量;
(2)酸性条件下,碘离子被氧气氧化生成碘单质;过量的碘离子易被空气氧化生成碘单质,导致测定结果偏大;
(3)酸性条件下,碘离子和碘酸根离子能发生氧化还原反应生成碘单质,淀粉遇碘变蓝色,根据溶液是否变蓝判断是否含有碘离子;
解答 解:(1)①Na2S2O3为强碱弱酸盐,因为硫代硫酸根离子水解,Na2S2O3溶液呈弱碱性,所以配制250mlNa2S2O3溶液需要的仪器除电子天平、玻璃棒、烧杯、胶头滴管外,还需250ml的容量瓶,
故答案为:250ml容量瓶;
②反应中生成I2,c中使用淀粉作为指示剂;加入淀粉,溶液呈蓝色,用Na2S2O3溶液滴定,I2反应完毕,溶液蓝色褪色,滴定终点现象为:溶液蓝色褪色,半分钟内不恢复蓝色;
20mL溶液消耗Na2S2O3的物质的量为1.00×10-3mol/L×0.02L=2.00×10-5mol,根据IO3-+5I-+6H+=3I2+3H2O,I2+2S2O32-=2I-+S4O62-,则:
IO3-~3I2~6S2O32-,
1 6
n 2.00×10-5mol
所以n=$\frac{2.00}{6}$×10-5mol=$\frac{1}{3}$×10-5mol,
故加碘食盐样品中的碘元素含量=$\frac{\frac{1}{3}×1{0}^{-5}mol×127g/mol}{14.1g}$×106mg/kg=30.0mg/kg,
故答案为:蓝,无;30.0;
(2)酸性条件下,碘离子被氧气氧化生成碘单质,离子反应方程式为:4I-+4H++O2=2I2+2H2O;且酸性条件下,过量的碘离子易被空气中氧气氧化生成碘单质,因b用稀硫酸酸化,再加入过量KI溶液,发生反应IO3-+5I-+6H+=3I2+3H2O,所以导致测定结果偏大,
故答案为:加H2SO4后,溶液中O2氧化KI生成I2与淀粉作用显蓝色,偏大;
(3)电解后的溶液区含有碘酸根离子,酸性条件下,碘离子和碘酸根离子能发生氧化还原反应IO3-+5I-+6H+=3I2+3H2O生成碘单质,淀粉溶液遇碘变蓝色,所以实验方法是:取少量阳极区电解液于试管中,加稀硫酸酸化后加入几滴淀粉溶液,观察是否变蓝;如果阳极区含有碘离子,加入稀硫酸后就有碘单质生成,淀粉溶液就会变蓝色,若溶液变蓝则电解不完全,若无明显现象则电解完全,
故答案为:
| 实验操作 | 实验现象及结论 |
| 取少量电解后的溶液于试管中,先滴加淀粉溶液,再滴加稀硫酸酸化 | 若溶液变蓝则电解不完全,若无明显现象则电解完全. |
点评 本题以碘酸钾中碘的测定为载体考查了氧化还原滴定的应用、对实验原理理解与实验装置的评价,注意掌握碘及其化合物的性质是解答本题的关键,题目难度中等.

| A. | 3s23p63d2 | B. | 2d10 | C. | 3s23p64s2 | D. | 3s23p33d5 |
| A. | 饮用水越纯净对人体越有益 | |
| B. | 调味剂和营养剂加得越多越好 | |
| C. | 垃圾分类有利于资源回收利用,废易拉罐不是有害垃圾,可回收利用 | |
| D. | 为消除碘缺乏症,卫生部规定必须在食盐中加碘单质 |
| A. | 16 | B. | 28 | C. | 32 | D. | 48 |

 .
.