题目内容
【题目】(13分)用辉铜矿(主要成分为 Cu2S,含少量Fe2O3、SiO2,等杂质)制备难溶于水的碱式碳酸铜的流程如下:
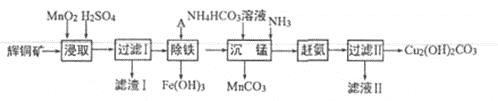
(1)下列措施是为了加快浸取速率,其中无法达到目的的是____(填字母)。
A.延长浸取时间 | B.将辉铜矿粉碎 |
C.充分搅拌 | D.适当增加硫酸浓度 |
(2)滤渣I巾的主要成分是MnO2、S、SiO2,请写出“浸取”反应中生成S的离子方程式:_______。
(3)研究发现,若先除铁再浸取,浸取速率明显变慢,可能的原因是___________。
(4)“除铁”的方法是通过调节溶液pH,使Fe3+转化为Fe(OH)3,则加入的试剂A可以是_______(填化学式);“赶氨”时,最适宜的操作方法是________。
(5)“沉锰”(除Mn2+)过程中有关反应的离子方程式为_______。
(6)滤液Ⅱ经蒸发结晶得到的盐主要是___________(填化学式)。
【答案】(1)A (2)2MnO2+Cu2S+8H+=S+2Cu2++2Mn2++4H2O (3)Fe3+可催化Cu2S被MnO2氧化
(4)CuO或Cu(OH)2;将溶液加热 (5)Mn2++HCO3-+NH3=NH4++MnCO3↓ (6)(NH4)2SO4
【解析】
试题(1)增大反应物的接触面积或升高温度等均可以增大反应速率,所以酸浸时,通过粉碎矿石或者升高温度或者进行搅拌都可以提高浸取率,但延长浸取时间并不能提高速率,答案选A。
(2)在酸性条件下MnO2氧化Cu2S得到硫沉淀、CuSO4、MnSO4和水,所以该反应的离子方程式是2MnO2+Cu2S+8H+=S+2Cu2++2Mn2++4H2O。
(3)由于Fe3+可催化Cu2S被MnO2氧化,所以若先除铁再浸取,浸取速率明显变慢。
(4)由于除杂时不能再引入新的杂质,所以加入的试剂A可以是CuO或Cu(OH)2。氨气易挥发,则“赶氨”时,最适宜的操作方法是将溶液加热。
(5)根据原子守恒可知“沉锰”(除Mn2+)过程中除了生成碳酸锰外还有铵盐生成,则有关反应的离子方程式为Mn2++HCO3-+NH3=NH4++MnCO3↓。
(6)滤液Ⅱ中含有硫酸铵,因此经蒸发结晶得到的盐主要是(NH4)2SO4。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】下表是元素周期表的一部分。表中所列的字母分别代表一种化学元素。
a | b | ||||||||||||||||
[ | c | d | e | f | |||||||||||||
g | h | i | j | k | l | m | |||||||||||
n | o |
请根据要求用元素符号或化学式回答下列问题:
(1)表中所列元素中,原子最外层有2个电子的元素为_________。
(2)画出d元素原子的结构示意图_______________________________,其气态氢化物溶于水显_____________性。(填“酸”或“碱”)
(3)比较元素g和元素h形成的最高价氧化物的水化物的碱性强弱________>__________。
(4)表中j元素在元素周期表中的位置是______________________。
(5)表中所列元素中,最高价氧化物对应水化物碱性最强的是___________(填写化合物的化学式,下同),具有两性的是_____________,
