题目内容
【题目】⑴在①NaCl、②NaOH、③N2、④H2S、⑤Na2O2中,只含有离子键的是________,只含有极性键的是______,既含离子键又含非极性共价键的是____。
(2)写出下列物质的电子式:
CO2____________NaCl____________ HClO_______________
【答案】① ④ ⑤ ![]()
![]()
![]()
【解析】
金属阳离子和阴离子之间的化学键为离子键,一般盐、碱金属氧化物中含有离子键,非金属元素之间的化学键为共价键,其中相同非金属元素形成的为非极性共价键,不同非金属元素形成的为极性共价键,根据化合物的类型写出电子式,据此进行判断。
(1)①NaCl为离子化合物,只含有离子键;
②NaOH为离子化合物,既含有离子键,又含有极性共价键;
③N2为非金属单质,只含有非极性共价键;
④H2S为共价化合物,只含有极性共价键;
⑤Na2O2为离子化合物,既含有离子键,又含有非极性共价键;
故:只含有离子键的是①,只含有极性键的是④,既含离子键又含非极性共价键的是⑤;
(2)CO2为共价化合物,电子式为![]() ;氮气分子内存在氮氮叁键,则其电子式为
;氮气分子内存在氮氮叁键,则其电子式为![]() ;HClO为共价化合物,电子式为
;HClO为共价化合物,电子式为![]() 。
。

 小学能力测试卷系列答案
小学能力测试卷系列答案【题目】(13分)用辉铜矿(主要成分为 Cu2S,含少量Fe2O3、SiO2,等杂质)制备难溶于水的碱式碳酸铜的流程如下:
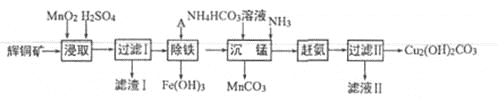
(1)下列措施是为了加快浸取速率,其中无法达到目的的是____(填字母)。
A.延长浸取时间 | B.将辉铜矿粉碎 |
C.充分搅拌 | D.适当增加硫酸浓度 |
(2)滤渣I巾的主要成分是MnO2、S、SiO2,请写出“浸取”反应中生成S的离子方程式:_______。
(3)研究发现,若先除铁再浸取,浸取速率明显变慢,可能的原因是___________。
(4)“除铁”的方法是通过调节溶液pH,使Fe3+转化为Fe(OH)3,则加入的试剂A可以是_______(填化学式);“赶氨”时,最适宜的操作方法是________。
(5)“沉锰”(除Mn2+)过程中有关反应的离子方程式为_______。
(6)滤液Ⅱ经蒸发结晶得到的盐主要是___________(填化学式)。
【题目】下列三个化学反应的平衡常数(K1、K2、K3)与温度的关系分别如下表所示:
化学反应 | 平衡常数 | 温度 | |
973K | 1173K | ||
①Fe(s)+CO2(g) | K1 | 1.47 | 2.15 |
②Fe(s)+H2O(g) | K2 | 2.38 | 1.67 |
③CO(g)+H2O(g) | K3 | ? | ? |
则下列说法正确的是
A.△H1<0,△H2>0
B.反应①②③的反应热满足关系:△H2-△H1=△H3
C.反应①②③的平衡常数满足关系:K1·K2=K3
D.要使反应③在一定条件下建立的平衡向正反应方向移动,可采取升温措施