题目内容
【题目】某混合溶液中所含离子的浓度如下表,则Mn+及a值可能为
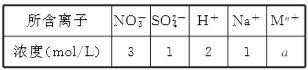
A. Mg2+、1 B. Ba2+、0.5 C. Al3+、1.5 D. Fe2+、2
【答案】A
【解析】
电解质混合溶液中阴阳离子所带电荷相等,故溶液中存在c(H+)+c(Na+)+nc(Mn+)=c(NO3-)+2c(SO42-),据此结合选项代入计算判断。
电解质混合溶液中阴阳离子所带电荷相等,故溶液中存在c(H+)+c(Na+)+ nc(Mn+)=c(NO3-)+2c(SO42-),故2mol/L+1mol/L+ nc(Mn+)=3mol/L+1mol/L![]() 2,故nc(Mn+)=2mol/L,
2,故nc(Mn+)=2mol/L,
A、1mol/L的Mg2+,2![]() 1mol/L =2mol/L,故A符合;
1mol/L =2mol/L,故A符合;
B、0.5mol/L的Ba2+,2![]() 0.5mol/L=1mol/L,且Ba2+与SO42-不能共存,故B不符合;
0.5mol/L=1mol/L,且Ba2+与SO42-不能共存,故B不符合;
C、1.5mol/L的Al3+,3![]() 1.5mol/L =4.5mol/L,故C不符合;
1.5mol/L =4.5mol/L,故C不符合;
D、2mol/L的Fe2+,2![]() 2mol/L=4mol/L,故D不符合。
2mol/L=4mol/L,故D不符合。
所以A选项是正确的。

 阅读快车系列答案
阅读快车系列答案【题目】温度分别为T1和T2时,将气体X和气体Y各0.16mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)![]() 2Z(g),一段时间后达到平衡,反应过程中测定的数据如下表:
2Z(g),一段时间后达到平衡,反应过程中测定的数据如下表:
温度/K | t/min | t1 | t2 | t3 | t4 |
T1 | n(Y)/mol | 0.14 | 0.12 | 0.10 | 0.10 |
T2 | n(Y)/mol | 0.13 | 0.09 | 0.08 |
下列说法正确的是( )
A. 该反应的正反应为放热反应
B. T2温度下此反应的平衡常数K=4
C. 温度为T1时,0~t1时间段的平均速率υ(Z)=2.0×10-3mol·L-1·min-1
D. 在T1下平衡后,保持其他条件不变,再充入0.2molZ,平衡时X的体积分数增大