题目内容
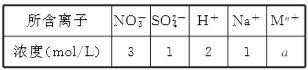
【题目】已知某条件下,SO2(g)和O2(g)反应生成2molSO3(g)时,放出的热量为QkJ。在1L的密闭容器中进行反应2SO2(g)+O2(g)![]() 2SO3(g),SO2、O2、SO3 的起始物质的量分别为 0.2mol、0.1mol、0.2mol,下列叙述正确的是
2SO3(g),SO2、O2、SO3 的起始物质的量分别为 0.2mol、0.1mol、0.2mol,下列叙述正确的是
A.某时刻,SO3的物质的量为0.28 mol,则SO2 的转化率为40%
B.反应达到平衡时放出的热量为0.1QkJ
C.反应正向进行时,混合物的平均摩尔质量减小
D.某时刻,SO3的浓度可能为0.3mol·L-1
【答案】AD
【解析】
A.SO3的起始物质的量为0.2mol,某时刻为0.28mol,则SO3生成了0.08mol,由方程式计量数可知,SO2也转化了0.08mol,SO2的转化率=![]() =40%,A正确;
=40%,A正确;
B.每生成2molSO3(g)时,放出的热量为QkJ,SO2、O2的起始物质的量分别为0.2mol、0.1mol,因为是可逆反应,生成SO3的物质的量一定小于0.2mol,故放出的热量少于0.1QkJ,B错误;
C.反应正向进行,气体总物质的量减小,总质量不变,由n=![]() 可知,M必然增大,即混合物的平均摩尔质量增大,C错误;
可知,M必然增大,即混合物的平均摩尔质量增大,C错误;
D.该反应是可逆反应,若反应正向进行,生成SO3的物质的量大于0,小于0.2mol,该时刻SO3的物质的量大于0.2mol,小于0.4mol,即可能为0.3mol,D正确。
答案选AD。

 走进文言文系列答案
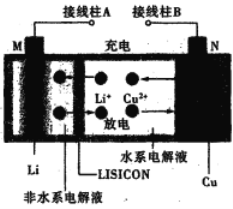
走进文言文系列答案【题目】为增强铝的耐腐蚀性,现以铅蓄电池为外电源,以Al作阳极、Pb作阴极,电解稀硫酸,使铝表面的氧化膜增厚。其反应原理如下: 电池: Pb(s) + PbO2(s) + 2H2SO4(aq) =2PbSO4(s) + 2H2O(l);
电解池:2Al+3O2![]() Al2O3+3H2↑电解过程中,以下判断正确的是( )
Al2O3+3H2↑电解过程中,以下判断正确的是( )
电池 | 电解池 | |
A | H+移向Pb电极 | H+移向Pb电极 |
B | 每消耗3molPb | 生成2molAl2O3 |
C | 正极:PbO2+4H++2e—=Pb2++2H2O | 阳极:2Al+3H2O-6e—=Al2O3+6H+ |
D |
|
|