题目内容
700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:CO(g)+H2O(g)  CO2+H2(g)反应过程中测定的部分数据见下表(表中t1>t2):
CO2+H2(g)反应过程中测定的部分数据见下表(表中t1>t2):
依据题意回答下列问题:
(1)反应在t1min内的平均速率为v(H2)= mol·L-1·min-1
(2)保持其他条件不变,起始时向容器中充入0.60molCO和1.20 molH2O,到达平衡时,n(CO2)= mol。
(3)保持其他条件不变,向平衡体系中再通入0.20molH2O,与原平衡相比,达到新平衡时CO转化率 (填“增大”或“减小”或“不变” 下同),H2O的体积分数
(4)温度升至800℃,该反应平衡常数为0.64,则正反应为 反应(填“放热”或“吸热”)。
 CO2+H2(g)反应过程中测定的部分数据见下表(表中t1>t2):
CO2+H2(g)反应过程中测定的部分数据见下表(表中t1>t2):| 反应时间/min | n(CO)/mol | n(H2O)/ mol |
| 0 | 1.20 | 0.60 |
| t1 | 0.80 | |
| t2 | | 0.20 |
(1)反应在t1min内的平均速率为v(H2)= mol·L-1·min-1
(2)保持其他条件不变,起始时向容器中充入0.60molCO和1.20 molH2O,到达平衡时,n(CO2)= mol。
(3)保持其他条件不变,向平衡体系中再通入0.20molH2O,与原平衡相比,达到新平衡时CO转化率 (填“增大”或“减小”或“不变” 下同),H2O的体积分数
(4)温度升至800℃,该反应平衡常数为0.64,则正反应为 反应(填“放热”或“吸热”)。
(1)0.20/t1 (2)0.40 (3)增大 增大 (4)放热
试题分析:(1)在化学反应中速率比等于反应方程式各物质的化学计量数之比。反应在t1min内的平均速率为v(H2)=V(CO)="(" 1.2-0.8)mol÷2L÷t1min=0.20/t1mol/( L·min).(2)CO(g)+H2O(g)
 CO2+H2.在t1时n(CO)=0.80mol.变化了0.4mol.则n(H2O)=0.2mol.n(CO2)=n(H2) =0.4mol.由于t2<t1.说明在t1时反应已经达到平衡。因为反应前后物质的量保持不变,保持其他条件不变,平衡常数不会改变,起始时向容器中充入0.60molCO和1.20 molH2O,与起始时向容器中充入0.60molH2O和1.20 molCO效果是一致的,到达平衡时,n(CO2)=0.40 mol。(3)在其它条件不变的情况下,增大某反应物的浓度,能使其它反应物的转化率提高,而它本身的转化率反而降低。保持其他条件不变,向平衡体系中再通入0.20mol H2O,即增大了反应物的浓度化学平衡向正反应方向移动。与原平衡相比,达到新平衡时CO转化率增大,对H2O来说。增大水蒸汽的浓度,平衡正向移动使水蒸气的浓度减小,但平衡移动消耗量远远小于加入量,所以水的的体积分数增大。(4)温度升至800℃,该反应平衡常数为0.64,减小。说明升高温度,化学平衡向逆反应方向移动。根据平衡移动原理:升高温度,化学平衡向吸热反应方向移动。逆反应是吸热反应,所以正反应是放热反应。
CO2+H2.在t1时n(CO)=0.80mol.变化了0.4mol.则n(H2O)=0.2mol.n(CO2)=n(H2) =0.4mol.由于t2<t1.说明在t1时反应已经达到平衡。因为反应前后物质的量保持不变,保持其他条件不变,平衡常数不会改变,起始时向容器中充入0.60molCO和1.20 molH2O,与起始时向容器中充入0.60molH2O和1.20 molCO效果是一致的,到达平衡时,n(CO2)=0.40 mol。(3)在其它条件不变的情况下,增大某反应物的浓度,能使其它反应物的转化率提高,而它本身的转化率反而降低。保持其他条件不变,向平衡体系中再通入0.20mol H2O,即增大了反应物的浓度化学平衡向正反应方向移动。与原平衡相比,达到新平衡时CO转化率增大,对H2O来说。增大水蒸汽的浓度,平衡正向移动使水蒸气的浓度减小,但平衡移动消耗量远远小于加入量,所以水的的体积分数增大。(4)温度升至800℃,该反应平衡常数为0.64,减小。说明升高温度,化学平衡向逆反应方向移动。根据平衡移动原理:升高温度,化学平衡向吸热反应方向移动。逆反应是吸热反应,所以正反应是放热反应。
练习册系列答案
相关题目
 2SO3(g),平衡混合体系中SO3的百分含量和温度的关系如右图所示,根据下图回答下列问题:
2SO3(g),平衡混合体系中SO3的百分含量和温度的关系如右图所示,根据下图回答下列问题: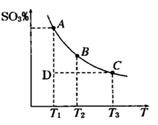
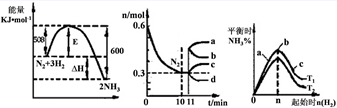
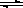 2N2O5(g)+5286 kJ已知体系中n(NO2)随时间变化如下表:
2N2O5(g)+5286 kJ已知体系中n(NO2)随时间变化如下表: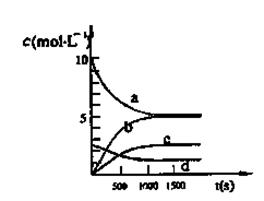
 2HBr(g) ΔH<0。当温度分别为T1、T2,平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示。下列说法正确的是
2HBr(g) ΔH<0。当温度分别为T1、T2,平衡时,H2的体积分数与Br2(g)的物质的量变化关系如图所示。下列说法正确的是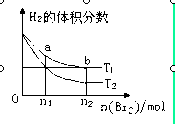
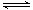 4NO2(g)+O2(g) ;⊿H>0
4NO2(g)+O2(g) ;⊿H>0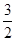 ,(不考虑NO2聚合成N2O4),则N2O5的转化率a1= ,该温度下反应的平衡常数K=_______。
,(不考虑NO2聚合成N2O4),则N2O5的转化率a1= ,该温度下反应的平衡常数K=_______。
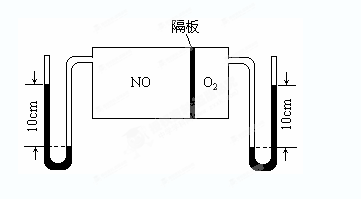
 CH3OH(g) ,其他条件不变,在300℃和500℃时,物质的量n(CH3OH)-反应时间t的变化曲线如图所示,下列说法正确的是
CH3OH(g) ,其他条件不变,在300℃和500℃时,物质的量n(CH3OH)-反应时间t的变化曲线如图所示,下列说法正确的是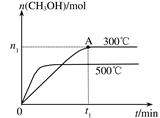
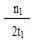 mol·L-1 min-1
mol·L-1 min-1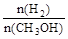 减小
减小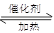 7N2(g)+12 H2O(g)可处理NO2。700℃时,向容积为2L的密闭容器中充入一定量的NO2和NH3, 反应过程中测定的部分数据见下表
7N2(g)+12 H2O(g)可处理NO2。700℃时,向容积为2L的密闭容器中充入一定量的NO2和NH3, 反应过程中测定的部分数据见下表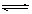 cC(g)+dD(g),达到平衡后将气体体积压缩到原来的一半,当再次达到新平衡时,D的浓度为原来的1.8倍,下列说法正确的是
cC(g)+dD(g),达到平衡后将气体体积压缩到原来的一半,当再次达到新平衡时,D的浓度为原来的1.8倍,下列说法正确的是 2C(g),经60 s达到平衡,生成0.6 mol C。下列说法正确的是
2C(g),经60 s达到平衡,生成0.6 mol C。下列说法正确的是