题目内容
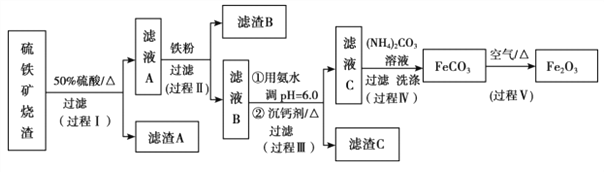
【题目】某课题组以硫铁矿烧渣(含 Fe2O3、 Fe3O4、 Al2O3、 CaO、 SiO2 等)为原料制取软磁用 Fe2O3(要求纯度>99.2%, CaO 含量<0.01%)。其工艺流程如下(所加入试剂均稍过量):
已知:生成氢氧化物的 pH 如下表所示
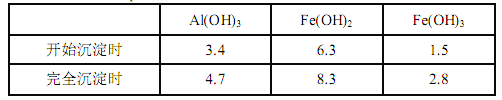
(1)滤渣 A 的主要成分是__________。
(2)在过程Ⅱ中可观察到产生少量气泡,溶液颜色慢慢变浅。能解释该实验现象的离子方程式有__________。
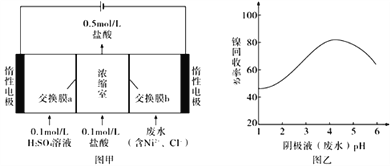
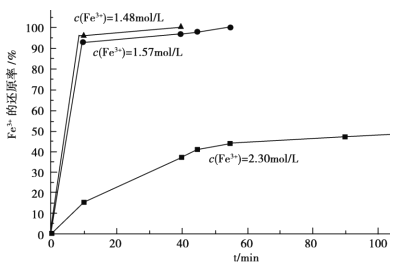
(3)在过程Ⅱ中,课题组对滤液 A 稀释不同倍数后,加入等质量的过量铁粉,得出 Fe3+浓度、还原率和反应时间的关系如图所示:结合上述实验结果说明:课题组选择稀释后c(Fe3+)为 1.60mol/L 左右的理由是______。
(4)在过程Ⅲ中,课题组在相同条件下,先选用了不同沉钙剂进行实验,实验数据见下表:(已知:滤液 B 中钙的含量以 CaO 计为 290—310mg/L)
沉钙剂 | Na2SO3 | H2C2O4 | (NH4)2CO3 | Na2CO3 | NH4F |
用量/g | 2 | 2 | 2 | 5 | 2 |
剩余CaO/mg/L) | 290 | 297 | 290 | 190 | 42 |
根据实验结果, 选择适宜的沉钙剂,得到滤渣 C 的主要成分有__________。
(5)在过程Ⅳ中,反应温度需要控制在 35℃以下,不宜过高,其可能的原因是__________。
(6)在过程Ⅴ中,反应的化学方程式是__________。
【答案】 SiO2 Fe+2H+=Fe2++H2↑ Fe+2Fe3+=3Fe2+ c(Fe3+)在1.60mol/L左右时,反应速率更快,Fe3+的还原率更高 CaF2、Al(OH)3 温度过高,(NH4)2CO3易分解 4FeCO3+O2![]() 2Fe2O3+4CO2↑
2Fe2O3+4CO2↑
【解析】试题分析:由题中流程可知,烧渣在加热的条件下经硫酸浸取后,过滤除去不溶物二氧化硅后,向滤液A中加入足量铁粉把Fe3+还原为Fe2+,过滤得滤液B,向滤液B中加入氨水调到pH=6.0,使Al3+完全转化为氢氧化铝沉淀,然后加入沉淀剂并加热,待滤液中Ca2+完全沉淀后过滤,向滤液C中加入碳酸铵溶液,过滤、洗涤,得到碳酸亚铁,最后将碳酸亚铁在空气中加热得到氧化铁。
(1)浇渣中只有SiO2不溶于硫酸,故滤渣 A 的主要成分是SiO2。
(2)在过程Ⅱ中可观察到产生少量气泡,溶液颜色慢慢变浅。该过程共有两个离子反应发生,其离子方程式为Fe+2Fe3+=3Fe2+、Fe+2H+=Fe2++H2↑。
(3)由Fe3+浓度、还原率和反应时间的关系曲线可知,c(Fe3+)在1.60mol/L左右时,反应速率更快(在很短的时间内达到很高的还原率),Fe3+的还原率更高,故课题组选择稀释后c(Fe3+)为 1.60mol/L左右。
(4)由表中实验数据可知,在相同的条件下,选择NH4F作为沉钙剂时,滤液B中钙的含量最低,故应选择NH4F作为沉钙剂,得到滤渣 C 的主要成分有CaF2、Al(OH)3。
(5)在过程Ⅳ中,使用了碳酸铵作为沉淀剂,反应温度需要控制在35℃以下,不宜过高,其可能的原因是:温度过高,(NH4)2CO3易分解。
(6)在过程Ⅴ中,碳酸亚铁在空气中加热得到氧化铁,反应的化学方程式是4FeCO3+O2![]() 2Fe2O3+4CO2↑ 。
2Fe2O3+4CO2↑ 。

【题目】实验室常利用甲醛法测定(NH4)2SO4样品中氮的质量分数,其反应原理为:4NH4+6HCHO===3H++6H2O+(CH2)6N4H+[滴定时,1 mol(CH2)6N4H+与1 mol H+相当],然后用NaOH标准溶液滴定反应生成的酸.某兴趣小组用甲醛法进行了如下实验:
步骤Ⅰ 称取样品1.500 g。
步骤Ⅱ 将样品溶解后,完全转移到250 mL容量瓶中,定容,充分摇匀。
步骤Ⅲ 移取25.00 mL样品溶液于250 mL锥形瓶中,加入10 mL 20%的中性甲醛溶液,摇匀、静置5 min后,加入1~2滴酚酞试液,用NaOH标准溶液滴定至终点。按上述操作方法再重复2次。
(1)根据步骤Ⅲ填空:
①碱式滴定管用蒸馏水洗涤后,直接加入NaOH标准溶液进行滴定,则测得样品中氮的质量分数________(填“偏高”、“偏低”或“无影响”)。
②锥形瓶用蒸馏水洗涤后,水未倒尽,则滴定时用去NaOH标准溶液的体积________(填“偏大”、“偏小”或“无影响”)。
③滴定时边滴边摇动锥形瓶,眼睛应观察____________________。
A.滴定管内液面的变化 B.锥形瓶内溶液颜色的变化
④滴定达到终点时,酚酞指示剂由______色变成____________色。
(2)滴定结果如下表所示:
滴定次数 | 待测溶液的体积/mL | 标准溶液的体积 | |
滴定前刻度/mL | 滴定后刻度/mL | ||
1 | 25.00 | 1.02 | 21.03 |
2 | 25.00 | 2.00 | 21.99 |
3 | 25.00 | 0.20 | 20.20 |
若NaOH标准溶液的浓度为0.1010 mol/L,则该样品中氮的质量分数为________。
【题目】对下列实验现象解释正确的是
实验内容 | 实验现象 | 相关解释 | |
A | 等量的Cu分别与等体积足量的浓硝酸和稀硝酸反应 | 浓硝酸反应后呈绿色,稀硝酸反应后呈蓝色 | c(Cu2+)不同 |
B | NH3与Cl2混合 | 生成白烟 | NH3与Cl2发生化合反应生成NH4Cl |
C | 往Fe(OH)3胶体中逐滴滴入稀盐酸 | 先出现红褐色沉淀,后沉淀溶解 | 先胶体聚沉,后Fe(OH)3溶解 |
D | 加热硝酸铜固体,将带火星的木条伸入所得的气体中 | 生成红棕色气体,带火星木条复燃 | 2Cu(NO3)2 |
A. A B. B C. C D. D