题目内容
氯酸镁[Mg(ClO3)2]常用作催熟剂、除草剂等,实验室用卤块(主要成分为MgCl2·6H2O,含有MgSO4、FeCl2等杂质)制备少量Mg(ClO3)2·6H2O的流程如下:

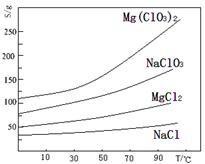
已知:几种化合物的溶解度(S)随温度(T)变化曲线如下图所示。
(1)过滤时主要玻璃仪器有 。加入BaCl2的目的是除去杂质离子,检验已沉淀完全的方法是: 。
(3)“调节pH=4”可选用的试剂是 (填编号)
①MgO ②CuO ③稀NaOH溶液
④Mg ⑤稀硫酸 ⑥MgCO3
(4)反应II为:MgCl2+2NaClO3=Mg(ClO3)2+2NaCl↓,再进一步制取Mg(ClO3)2·6H2O的实验步骤依次为:① ;②趁热过滤;③ ;④过滤、洗涤、干燥。
(5)产品中Mg(ClO3)2·6H2O含量的测定:
步骤1:准确称量m g产品配成100 mL溶液。
步骤2:取10 mL溶液于锥形瓶中,加入10 mL稀硫酸和20 mL 1.000 mol·L-1的FeSO4溶液,微热。
步骤3:冷却至室温,用0.100 mol·L-1 K2Cr2O7标准溶液滴定未被氧化的Fe2+。记录消耗K2Cr2O7溶液的体积。
①步骤2中发生反应的离子方程式为: 。
②若配制K2Cr2O7标准溶液时未洗涤烧杯,则产品中Mg(ClO3)2·6H2O的含量会 。(填“偏高”、“偏低” 或“不变”)。

已知:几种化合物的溶解度(S)随温度(T)变化曲线如下图所示。

(1)过滤时主要玻璃仪器有 。加入BaCl2的目的是除去杂质离子,检验已沉淀完全的方法是: 。
(3)“调节pH=4”可选用的试剂是 (填编号)
①MgO ②CuO ③稀NaOH溶液
④Mg ⑤稀硫酸 ⑥MgCO3
(4)反应II为:MgCl2+2NaClO3=Mg(ClO3)2+2NaCl↓,再进一步制取Mg(ClO3)2·6H2O的实验步骤依次为:① ;②趁热过滤;③ ;④过滤、洗涤、干燥。
(5)产品中Mg(ClO3)2·6H2O含量的测定:
步骤1:准确称量m g产品配成100 mL溶液。
步骤2:取10 mL溶液于锥形瓶中,加入10 mL稀硫酸和20 mL 1.000 mol·L-1的FeSO4溶液,微热。
步骤3:冷却至室温,用0.100 mol·L-1 K2Cr2O7标准溶液滴定未被氧化的Fe2+。记录消耗K2Cr2O7溶液的体积。
①步骤2中发生反应的离子方程式为: 。
②若配制K2Cr2O7标准溶液时未洗涤烧杯,则产品中Mg(ClO3)2·6H2O的含量会 。(填“偏高”、“偏低” 或“不变”)。
(1)漏斗、玻璃棒、烧杯
(2)静置,取上层清液加入BaCl2,若无白色沉淀,则SO42-沉淀完全
(3)①③⑥
(4)蒸发浓缩 冷却结晶
(5)①ClO3-+6Fe2++6H+=6Fe3++Cl-+3H2O ②偏低
试题分析:(1)过滤实验用到的仪器:漏斗、玻璃棒、烧杯、滤纸、铁架台等,其中玻璃仪器有:漏斗、玻璃棒、烧杯。(2)根据Ba2+可以和SO42-离子之间反应生成白色不溶于硝酸的白色BaSO4沉淀,检验硫酸根离子是否除净的方法:静置,取上层清液加入BaCl2,若无白色沉淀,则SO42-沉淀完全。
(3)反应I中H2O2的作用是将Fe2+氧化为Fe3+,由于Fe3+→Fe(OH)3↓的pH≈3,所以调节pH=4的目的是使Fe3+→Fe(OH)3↓而除去;为了不引入新的杂质应选MgO或MgCO3,此外,由于Ksp[Fe(OH)3]<Ksp[Mg(OH)2],NaCl可通过降温结晶法与Mg(ClO3)2分离,所以选则NaOH亦可。
(4)根据题给图像可知:Mg(ClO3)2溶解度随温度变化较大,溶液获得晶体的方法可采用蒸发结晶、过滤、冷却结晶。(5)①ClO3-离子具有氧化性,可以将Fe2+氧化为Fe3+,根据氧化还原反应配平即可。②根据ClO3-+6Fe2++6H+=6Fe3++Cl-+3H2O、Cr2O72-+6Fe2++14H+═2Cr3++6Fe3++7H2O,可以得出:ClO3-~6Fe2+,Cr2O72-~6Fe2+,若配制K2Cr2O7标准溶液时未洗涤烧杯,则K2Cr2O7浓度偏低,剩余Fe2+含量偏高,由于铁的总量一定,所以则产品中 Mg(ClO3)2的含量会偏低。
知识解决简单化学问题的能力以及对图表的观察、分析能力,物质溶解度概念的应用,晶体析出的方
法,杂质离子的除杂原则和试剂选择,题目难度中等.。

练习册系列答案
相关题目