题目内容
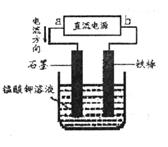
由于Fe (OH)2极易被氧化,所以实验室很难用亚铁盐溶液与烧碱反应制得白色纯净的Fe (OH)2沉淀,应用下图电解实验可以制得白色的纯净的Fe (OH)2沉淀。两电极材料分别为石墨和铁。

(1)b电极材料应为____,电极反应式为________________。
(2)电解液C可以是__________。

(1)b电极材料应为____,电极反应式为________________。
(2)电解液C可以是__________。
| A.纯净水 | B.NaCl溶液 | C.NaOH溶液 | D.CuCl2溶液 |
(1)铁,Fe-2e =" Fe" 2+ (2)B、C
试题分析:(1)b极为阳极,发生氧化反应,铁单质失去电子,电极反应式为Fe-2e- =" Fe" 2+;(2)电解液必须是电解质溶液,A错误;电解NaCl溶液,阳极为铁单质被氧化,阴极为氢离子在放电,故溶液中存在着由水电离出来的氢氧根离子,则与亚铁离子结合,生成氢氧化亚铁沉淀,B正确;电解氢氧化钠溶液,阳极为铁单质被氧化,生成的亚铁离子与溶液中的氢氧根离子结合,生成氢氧化亚铁沉淀,阴极为氢离子在放电,C符合要求;电解氯化铜溶液,阳极为铁单质被氧化,阴极为铜离子在放电,在石墨表面附着铜,亚铁离子存在电解液中,D不符合要求。
点评:电解池是历年高考常考知识点,注重考查学生分析问题、解决问题的能力。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目