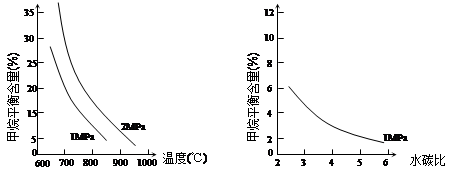题目内容
I.工业上可用CO生产燃料甲醇。一定条件下发生反应:CO(g)+2H2(g) CH3OH(g)
CH3OH(g)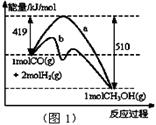
(1)“图1”表示反应中能量的变化,曲线 (填“a或b”)表示使用了催化剂;该反应的热化学方程式为 。
(2)若容器容积不变,下列措施可增大CO平衡转化率的是_____。
| A.升高温度 |
| B.将CH3OH(g)从体系中分离 |
| C.充入He,使体系总压强增大 |
| D.再充入1 mol CO和2 mol H2 |
II.向BaSO4沉淀中加入饱和碳酸钠溶液,充分搅拌,弃去上层清液,如此处理多次,可使BaSO4全部转化为BaCO3,发生的反应可表示为:BaSO4(s)+CO32-(aq)
 BaCO3(s)+SO42-(aq)。
BaCO3(s)+SO42-(aq)。(4)现有0.20 mol BaSO4,加入1.0L 2.0mol/L的饱和Na2CO3溶液处理,假设起始的c(SO42-)≈0,平衡时,K=4.0×10-2,求达到平衡时发生转化的BaSO4的物质的量。(写出计算过程,计算结果保留2位有效数字)
(16分)
(1)b(1分)
CO(g)+2H2(g) CH3OH(g) △H=-91kJ/mol (3分,方程式含状态符号正确给1分;反应热2分,其中单位写错扣1分,但结果或符号写错不给分,可逆符号也可以写成等号)
CH3OH(g) △H=-91kJ/mol (3分,方程式含状态符号正确给1分;反应热2分,其中单位写错扣1分,但结果或符号写错不给分,可逆符号也可以写成等号)
(2)BD(4分,答对1个给2分,但错选不给分)
(3)如图(2分,作图1分,标注1分)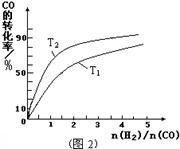
(4)解:设发生转化的BaSO4的物质的量为x mol ,则平衡时c(SO42-)为x mol/L
BaSO4 + CO32-  BaCO3 + SO42-
BaCO3 + SO42-
起始浓度/mol?L-1 2.0 0
变化浓度/mol?L-1 x x
平衡浓度/mol?L-1 2.0-x x
K= =
=  = 4.0×10-2(2分,单位无写不扣分)
= 4.0×10-2(2分,单位无写不扣分)
解得:x = 7.7×10-2 (或0.077) 即发生转化的BaSO4的物质的量为7.7×10-2 mol。(2分,单位及有效数字错误各扣1分)
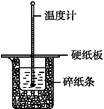
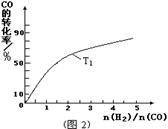
解析试题分析:(1)读图,反应物能量高于生成物能量,该反应的焓变为-91kJ/mol,曲线b有2个峰,a只有1个峰,且前者的2个峰均低于后者的1个峰,说明b使用了催化剂,将1个化学反应变为2个先后或连续发生的化学反应,且降低了反应的活化能,但是对总反应的焓变无影响,所以该反应的热化学方程式为CO(g)+2H2(g) CH3OH(g) △H=-91kJ/mol;(2)由于正反应是放热反应,其它条件相同时,升高温度平衡向逆反应方向移动,则CO平衡转化率减小,故A错误;甲醇是生成物,从平衡体系移走生成物,减小生成物浓度,平衡向正反应方向移动,反应物平衡转化率增大,故B正确;由于容器容积不变,虽然充入氦气增大压强,但是平衡体系各组分的物质的量、物质的量浓度均不变,所以平衡不能移动,反应物平衡转化率保持不变,故C错误;再充入1molCO和2molH2,就是增大压强,由于正反应是气体体积减小的反应,增大压强平衡向正反应方向移动,反应物的平衡转化率增大,故D正确;(3)读图,横坐标表示氢气和一氧化碳的起始组成比,纵坐标表示CO的平衡转化率;当氢气和一氧化碳的起始组成比为0时,CO的平衡转化率为0;当氢气和一氧化碳的起始组成比相同且不为零时,由于正反应是放热反应,降低温度平衡向正反应方向移动,CO的平衡转化率增大;当氢气和一氧化碳的起始组成比增大时,增大氢气的浓度,平衡向正反应方向移动,CO的平衡转化率增大;根据上述要点作图,可以画出温度为T2时,CO的平衡转化率随氢气和一氧化碳的起始组成比变化的示意图;(4)设硫酸钡溶解的物质的量为xmol,由于BaSO4 + CO32-
CH3OH(g) △H=-91kJ/mol;(2)由于正反应是放热反应,其它条件相同时,升高温度平衡向逆反应方向移动,则CO平衡转化率减小,故A错误;甲醇是生成物,从平衡体系移走生成物,减小生成物浓度,平衡向正反应方向移动,反应物平衡转化率增大,故B正确;由于容器容积不变,虽然充入氦气增大压强,但是平衡体系各组分的物质的量、物质的量浓度均不变,所以平衡不能移动,反应物平衡转化率保持不变,故C错误;再充入1molCO和2molH2,就是增大压强,由于正反应是气体体积减小的反应,增大压强平衡向正反应方向移动,反应物的平衡转化率增大,故D正确;(3)读图,横坐标表示氢气和一氧化碳的起始组成比,纵坐标表示CO的平衡转化率;当氢气和一氧化碳的起始组成比为0时,CO的平衡转化率为0;当氢气和一氧化碳的起始组成比相同且不为零时,由于正反应是放热反应,降低温度平衡向正反应方向移动,CO的平衡转化率增大;当氢气和一氧化碳的起始组成比增大时,增大氢气的浓度,平衡向正反应方向移动,CO的平衡转化率增大;根据上述要点作图,可以画出温度为T2时,CO的平衡转化率随氢气和一氧化碳的起始组成比变化的示意图;(4)设硫酸钡溶解的物质的量为xmol,由于BaSO4 + CO32-  BaCO3 + SO42-中各物质的系数之比等于物质的量之比,则碳酸根离子、硫酸根离子的变化物质的量均为xmol,由于饱和碳酸钠溶液的体积为1L,由于c=n/V,则碳酸根离子、硫酸根离子的变化物质的量浓度均为xmol/L,由此推断该可逆反应中有关组分的(起始、变化、平衡)浓度,则:
BaCO3 + SO42-中各物质的系数之比等于物质的量之比,则碳酸根离子、硫酸根离子的变化物质的量均为xmol,由于饱和碳酸钠溶液的体积为1L,由于c=n/V,则碳酸根离子、硫酸根离子的变化物质的量浓度均为xmol/L,由此推断该可逆反应中有关组分的(起始、变化、平衡)浓度,则:
BaSO4 + CO32-  BaCO3 + SO42-
BaCO3 + SO42-
起始浓度/mol?L-1 2.0 0
变化浓度/mol?L-1 x x
平衡浓度/mol?L-1 2.0-x x
K= =
=  = 4.0×10-2
= 4.0×10-2
解得:x = 7.7×10-2 (或0.077)
即发生转化的BaSO4的物质的量为7.7×10-2 mol。
考点:考查化学反应原理,涉及催化剂对反应体系能量的影响、根据图像书写热化学方程式、外界条件对平衡移动的影响、画出CO平衡转化率随温度、反应物起始配比变化的示意图、沉淀转化中的有关平衡常数和沉淀转化量的计算等。

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 某市对大气进行监测,发现该市首要污染物为可吸入颗粒物PM2.5(直径小于等于2.5μm的悬浮颗粒物),其主要来源为燃煤、机动车尾气等。因此,对PM2.5、SO2、NOx等进行研究具有重要意义。
请回答下列问题:
(1)将PM2.5样本用蒸馏水处理制成待测试样。
若测得该试样所含水溶性无机离子的化学组分及其平均浓度如下表:
| 离子 | K+ | Na+ | N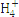 | S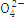 | N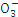 | Cl- |
| 浓度/mol·L-1 | 4×10-6 | 6×10-6 | 2×10-5 | 4×10-5 | 3×10-5 | 2×10-5 |
(2)为减少SO2的排放,常采取的措施有:
①将煤转化为清洁气体燃料。
已知:H2(g)+
 O2(g) H2O(g) ΔH="-241.8" kJ·mol-1 ①
O2(g) H2O(g) ΔH="-241.8" kJ·mol-1 ①C(s)+
 O2(g) CO(g) ΔH="-110.5" kJ·mol-1 ②
O2(g) CO(g) ΔH="-110.5" kJ·mol-1 ②写出焦炭与水蒸气反应的热化学方程式: 。
②洗涤含SO2的烟气。以下物质可作洗涤剂的是 。
a.Ca(OH)2 b.Na2CO3 c.CaCl2 d.NaHSO3
(3)汽车尾气中NOx和CO的生成及转化
①已知汽缸中生成NO的反应为:
N2(g)+O2(g)
 2NO(g) ΔH>0
2NO(g) ΔH>0若1 mol空气含0.8 mol N2和0.2 mol O2,1 300℃时在密闭容器内反应达到平衡,测得NO为8×10-4mol。计算该温度下的平衡常数K= 。
汽车启动后,汽缸温度越高,单位时间内NO排放量越大,原因是 。
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:
2CO(g) 2C(s)+O2(g)
已知该反应的ΔH>0,简述该设想能否实现的依据:
。
③目前,在汽车尾气系统中装置催化转化器可减少CO和NO的污染,其化学反应方程式为 。
在密闭容器中,存在反应: ,下列可使化学反应速率增大的措施是( )
,下列可使化学反应速率增大的措施是( )
A.减小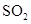 浓度 浓度 | B.升高温度 | C.增大容器体积 | D.降低温度 |
 CO(NH2)2(l)+H2O(g)在合成塔中进行。下图中Ⅰ、Ⅱ、Ⅲ三条曲线为合成塔中按不同氨碳比 [n(NH3)/n(CO2)]和水碳比[n(H2O)/n(CO2)]投料时二氧化碳转化率的情况。
CO(NH2)2(l)+H2O(g)在合成塔中进行。下图中Ⅰ、Ⅱ、Ⅲ三条曲线为合成塔中按不同氨碳比 [n(NH3)/n(CO2)]和水碳比[n(H2O)/n(CO2)]投料时二氧化碳转化率的情况。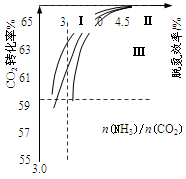
 CH3OH(g)。
CH3OH(g)。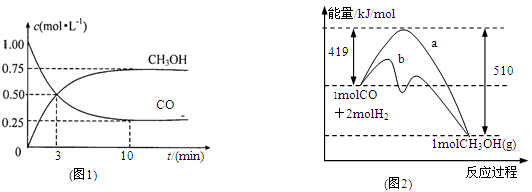
 增大的有
增大的有 
 CH3OH(g) ΔH1
CH3OH(g) ΔH1