题目内容
下列说法中正确的是
O2 反应放出115.6 kJ热量,键能如下表所示,则断裂1 mol
H-O键与断裂1 mol H-Cl键所需能量差为31.9 kJ

| A.生成物总能量一定低于反应物总能量 |
B.同温同压下,H2(g)+Cl2(g)=2HCl(g) 在光照和点燃条件下的 H不同 H不同 |
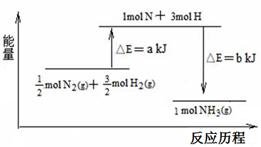
C.一定条件下,0.5 mol N2和1.5 mol H2置于某密闭容器中充分反应生成NH3气,放热19.3 kJ,其热化学方程式为N2(g)+3H2(g) 2NH3(g) 2NH3(g)  H =-38.6 kJ/mol H =-38.6 kJ/mol |
| D.一定条件下4 HCl(g)+O2(g)=2Cl2(g)+2H2O(g) ,当1 mol |
H-O键与断裂1 mol H-Cl键所需能量差为31.9 kJ

D
试题分析:A、在放热反应中生成物总能量一定低于反应物总能量,而在吸热反应中正好相反,错误;B、同一化学反应方程式相同条件下的
 H相同,错误;C、0.5 mol N2和1.5 mol H2置于某密闭容器中充分反应,反应物未全部转化为生成物,1mol氮气完全转化为氨气放出的热量应大于38.6kJ,所以N2(g)+3H2(g)
H相同,错误;C、0.5 mol N2和1.5 mol H2置于某密闭容器中充分反应,反应物未全部转化为生成物,1mol氮气完全转化为氨气放出的热量应大于38.6kJ,所以N2(g)+3H2(g) 2NH3(g)
2NH3(g)  H <-38.6 kJ/mol,错误;D、1 molO2 反应放出115.6 kJ热量,说明该反应的
H <-38.6 kJ/mol,错误;D、1 molO2 反应放出115.6 kJ热量,说明该反应的 H=-115.6kJ/mol,根据
H=-115.6kJ/mol,根据 H=反应物的总键能-生成物的总键能=4EH-Cl+498 kJ/mol -(2×243 kJ/mol +4×EO-H)= -115.6kJ/mol,解得EH-Cl- EO-H="-31.9" kJ/mol,正确,答案选D。
H=反应物的总键能-生成物的总键能=4EH-Cl+498 kJ/mol -(2×243 kJ/mol +4×EO-H)= -115.6kJ/mol,解得EH-Cl- EO-H="-31.9" kJ/mol,正确,答案选D。
练习册系列答案
 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案
相关题目
 AX5(g)在容积为10 L的密闭容器中进行。起始时AX3和X2均为0.2 mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。
AX5(g)在容积为10 L的密闭容器中进行。起始时AX3和X2均为0.2 mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。

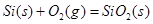 ;
;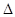 H="-989.2"
H="-989.2" 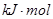
 则x的值为 ( )
则x的值为 ( )  O2(g) = NO2-(aq) + 2H+(aq) + H2O(l) ΔH = -273kL/mol
O2(g) = NO2-(aq) + 2H+(aq) + H2O(l) ΔH = -273kL/mol O2(g) = NO3-(aq) ΔH = -73kL/mol
O2(g) = NO3-(aq) ΔH = -73kL/mol
 2S(s) + 2H2O(g) ΔH= -442.38 kJ/mol ①
2S(s) + 2H2O(g) ΔH= -442.38 kJ/mol ①