题目内容
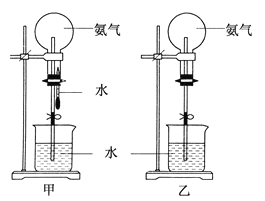
【题目】根据反应8NH3+3Cl2===6NH4Cl+N2,回答下列问题:
(1)该反应的氧化剂是_______________ ,还原剂是________________。
(2)氧化剂与还原剂的物质的量之比为________________。
(3)当有34 g NH3被氧化时,参加反应的氯气的质量为________________。
【答案】 Cl2 NH3 3∶2 213g
【解析】(1)8NH3+3Cl2=6NH4Cl+N2,反应中N元素化合价由-3价变为0价,化合价升高被氧化,Cl元素化合价由0价变为-1价,化合价降低被还原,所以NH3是还原剂、Cl2是氧化剂,故答案为:Cl2;NH3;
(2)该中N元素化合价由-3价变为0价、氯元素化合价由0价变为-1价,3mol氧化剂与2mol还原剂转移电子相等,则氧化剂与还原剂的物质的量之比为3:2,故答案为:3:2;
(3)n(NH3)= ![]() =2moL,氧化剂与还原剂的物质的量之比为3:2,则参加反应的氯气的质量为3mol,质量为3mol×71g/mol=213g,故答案为:213g。
=2moL,氧化剂与还原剂的物质的量之比为3:2,则参加反应的氯气的质量为3mol,质量为3mol×71g/mol=213g,故答案为:213g。

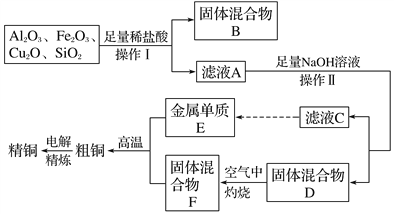
【题目】另一化学研究性学习小组在实验室条件下用以硫酸铜溶液为电解液,用电解的方法实现了粗铜的提纯,并对阳极泥和电解液中金属进行回收和含量测定.已知粗铜中含有少量的锌、铁、银、金等金属和少量矿物杂质(与酸不反应).
(1)步骤一:电解精制:电解时,粗铜应与电源的极相连.阴极上的电极反应式为 .
(2)步骤二:电解完成后,该小组同学按以下流程对电解液进行处理: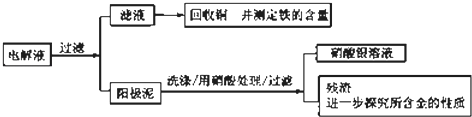
①阳极泥的综合利用:稀硝酸处理阳极泥得到硝酸银稀溶液,请写出该步反应的离子方程式: , 残渣含有极少量的黄金,如何回收金,他们查阅了有关资料,了解到了一些有关金的信息:
序号 | 反应 | 平衡常数 |
1 | Au+6HNO3Au(NO3)3+3NO2↑+3H2O | <<1 |
2 | Au3++4Cl﹣AuCl4- | >>1 |
请根据以上信息简要解释溶解阳极泥不用王水的原因 .
②滤液含量的测定:以下是该小组探究滤液的一个实验流程.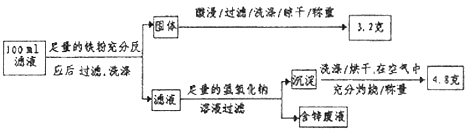
则100mL滤液中Cu2+的浓度为 molL﹣1 , Fe2+的浓度为 molL﹣1 .