题目内容
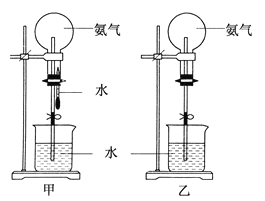
【题目】下图为氨气喷泉实验的装置:
(1)写出实验室制取NH3的化学方程式:_______________________________。
(2)收集氨气应使用_______法,要得到干燥的氨气可选用____________ 做干燥剂。
(3)用甲图装置进行喷泉实验,烧瓶已装满干燥的氨气,引发水向上喷的操作是________________。该实验的原理是____________________________________。
(4)如果只提供乙图装置,请说明引发喷泉的方法:_________________________。
【答案】 2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O 向下排空气法 碱石灰 打开止水夹,挤压滴管胶头使滴管内的水进入烧瓶 胶头滴管中挤出的水溶解了烧瓶里的氨气,使烧瓶中气体的压强迅速减小,远远小于外界的大气压时,烧杯中的水在内外压强差的作用下被压入烧瓶形成喷泉 打开止水夹,用双手(或热毛巾)捂住烧瓶使烧瓶内气体膨胀放出少量气体
CaCl2+2NH3↑+2H2O 向下排空气法 碱石灰 打开止水夹,挤压滴管胶头使滴管内的水进入烧瓶 胶头滴管中挤出的水溶解了烧瓶里的氨气,使烧瓶中气体的压强迅速减小,远远小于外界的大气压时,烧杯中的水在内外压强差的作用下被压入烧瓶形成喷泉 打开止水夹,用双手(或热毛巾)捂住烧瓶使烧瓶内气体膨胀放出少量气体
【解析】(1)氯化铵和氢氧化钙发生复分解反应,生成氯化钙、氨气和水,反应方程式为:2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O,故答案为:2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O,故答案为:2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O;
CaCl2+2NH3↑+2H2O;
(2)由于氨气密度比空气小、极易溶于水的性质,所以不能采用排水法收集,只能用向下排空气法的收集;反应过程中会产生水,使氨气中混有水蒸气,可用碱石灰吸收水蒸气,但不能用氯化钙和浓硫酸干燥,因为它们均与氨气反应,故答案为:向下排空气;碱石灰;
(3)氨气极易溶于水,如果打开止水夹,氨气溶于水后烧瓶内压强迅速减小,而形成喷泉,
故答案为:打开止水夹,挤出胶头滴管中的水;氨极易溶解于水,致使烧瓶内气体压强迅速减小,烧杯中的水在内外压强差的作用下被压入烧瓶形成喷泉;
(4)加热时烧瓶内压强增大,气体体积膨胀,当氨气与水接触时,因氨气极易溶于水而导致烧瓶内压强迅速减小而形成喷泉,故答案为:打开止水夹,用双手(或热毛巾)捂住烧瓶使烧瓶内气体膨胀放出少量气体。

【题目】由A、B、C、D四种金属按下表中装置进行实验.
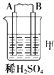
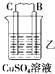
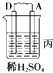
装置 |
|
|
|
现象 | 二价金属A不断溶解 | C的质量增加 | A上有气体产生 |
根据实验现象回答下列问题:
(1)装置甲中负极的电极反应式是 .
(2)装置乙中正极的电极反应式是 .
(3)装置丙中溶液的pH(填“变大”、“变小”或“不变”).
(4)四种金属活泼性由强到弱的顺序是 .