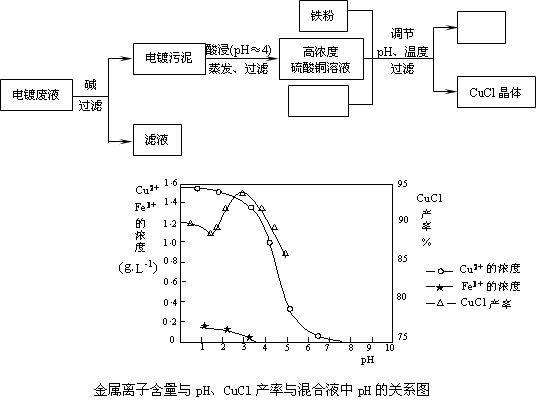
题目内容
(15分)水是生命之源,广西重金属镉污染事件是2012年1月15日发现的。水污染事件再次提醒人们保护水资源的必要性和紧迫性。工业废水中常含有一定量的Cr2O和CrO,它们会对人类及生态系统产生很大危害,必须进行处理。常用的处理方法有两种。
方法1:还原沉淀法。
该法的工艺流程为:
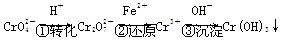
其中第①步存在平衡:
2CrO(黄色)+2H+ Cr2O(橙色)+H2O
Cr2O(橙色)+H2O
(1)若平衡体系的 pH = 2,该溶液显________色。
(2)能说明第①步反应达平衡状态的是________。(填序号)
A.Cr2O和CrO的浓度相同
B.2v(Cr2O)=v(CrO)
C.溶液的颜色不变
(3)第②步中,还原 1 mol Cr2O离子,需要______mol的FeSO4·7H2O。
(4)第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s) Cr3+(aq)+3OH-(aq)
Cr3+(aq)+3OH-(aq)
常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH-)=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至________。
方法2:电解法。
该法用 Fe 做电极电解含Cr2O的酸性废水,随着电解的进行,在阴极附近溶液 pH 升高,产生 Cr(OH)3沉淀。
(5)用Fe做电极的原因为__ __(用电极反应式解释)。
(6)在阴极附近溶液 pH 升高,溶液中同时生成的沉淀还有________。(用化学式表示)
(7)溶液中发生的总反应为(用离子方程式表示) 。
方法1:还原沉淀法。
该法的工艺流程为:
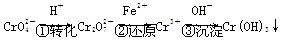
其中第①步存在平衡:
2CrO(黄色)+2H+
 Cr2O(橙色)+H2O
Cr2O(橙色)+H2O(1)若平衡体系的 pH = 2,该溶液显________色。
(2)能说明第①步反应达平衡状态的是________。(填序号)
A.Cr2O和CrO的浓度相同
B.2v(Cr2O)=v(CrO)
C.溶液的颜色不变
(3)第②步中,还原 1 mol Cr2O离子,需要______mol的FeSO4·7H2O。
(4)第③步生成的Cr(OH)3在溶液中存在以下沉淀溶解平衡:
Cr(OH)3(s)
 Cr3+(aq)+3OH-(aq)
Cr3+(aq)+3OH-(aq)常温下,Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH-)=10-32,要使c(Cr3+)降至10-5mol/L,溶液的pH应调至________。
方法2:电解法。
该法用 Fe 做电极电解含Cr2O的酸性废水,随着电解的进行,在阴极附近溶液 pH 升高,产生 Cr(OH)3沉淀。
(5)用Fe做电极的原因为__ __(用电极反应式解释)。
(6)在阴极附近溶液 pH 升高,溶液中同时生成的沉淀还有________。(用化学式表示)
(7)溶液中发生的总反应为(用离子方程式表示) 。
(15分)除第(7)3分外,其余每空均为2分。
(1)橙 (2)C (3)6 (4)5
(5)阳极反应为 Fe-2e-===Fe2+
(6) Fe(OH)3
(7) 6Fe2++Cr2O72-+10OH-+7H2O=6Fe(OH)3↓+2Cr(OH)3↓(3分)
(1)橙 (2)C (3)6 (4)5
(5)阳极反应为 Fe-2e-===Fe2+
(6) Fe(OH)3
(7) 6Fe2++Cr2O72-+10OH-+7H2O=6Fe(OH)3↓+2Cr(OH)3↓(3分)
方法1:还原沉淀法。
若平衡体系的 pH = 2,相当于在平衡中加入酸,平衡右移,显橙色。溶液的颜色不变说明第①步反应达平衡状态;第②步中,还原 1 mol Cr2O离子变为2molCr3+转移6mol电子,每摩尔亚铁离子转移1mol电子,需要6mol的FeSO4·7H2O。
Ksp=c(Cr3+)·c3(OH-)=10-32,要使c(Cr3+)降至10-5mol/L, c3(OH-)= 10-32/10-5=10-27
c(OH-)=10-9 mol/L,PH=5
方法2:电解法。
(5)用Fe做电极的原因为阳极反应为 Fe-2e-===Fe2+
(6) Cr2O还原Fe2+生成铁离子,与氢氧根生成Fe(OH)3。
(7)溶液中发生的总反应为6Fe2++Cr2O72-+10OH-+7H2O=6Fe(OH)3↓+2Cr(OH)3↓
若平衡体系的 pH = 2,相当于在平衡中加入酸,平衡右移,显橙色。溶液的颜色不变说明第①步反应达平衡状态;第②步中,还原 1 mol Cr2O离子变为2molCr3+转移6mol电子,每摩尔亚铁离子转移1mol电子,需要6mol的FeSO4·7H2O。
Ksp=c(Cr3+)·c3(OH-)=10-32,要使c(Cr3+)降至10-5mol/L, c3(OH-)= 10-32/10-5=10-27
c(OH-)=10-9 mol/L,PH=5
方法2:电解法。
(5)用Fe做电极的原因为阳极反应为 Fe-2e-===Fe2+
(6) Cr2O还原Fe2+生成铁离子,与氢氧根生成Fe(OH)3。
(7)溶液中发生的总反应为6Fe2++Cr2O72-+10OH-+7H2O=6Fe(OH)3↓+2Cr(OH)3↓

练习册系列答案
相关题目
 4Ag+O2↑
4Ag+O2↑ 2Fe+3CO2↑
2Fe+3CO2↑ Mg+C12↑
Mg+C12↑