��Ŀ����
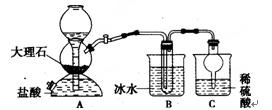
��������ҵ��ϴ�ֲ�ʱ�����ķ�Һ��Ҫ�ɷ�ΪFe2+��H+��Cl���������������������÷�Һ���������ᣬ�Ʊ�������Ϳ�ϡ� 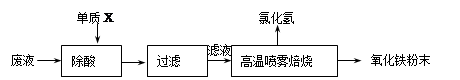
��1������X�Ļ�ѧʽ�� ��
��2���Ȼ�������Һ��������������ʱת��Ϊ�Ȼ����������������ĩ���йصĻ�ѧ����ʽΪ��
��3��ij������Ϳ�ϵijɷ��У�������Fe2O3�⣬��������CuO��FeO�е�һ�֡������ʵ��̽��������Ϳ�������ӵ����ʡ�
�������������
����1��������CuO�� ����2��������FeO��
�ڻ��ڼ��� ���1����2���������ʵ�鷽��������ʵ�顣�ڴ����д��ʵ�鲽�衢Ԥ������ͽ��ۡ�
��ѡʵ���Լ������ۡ�3mol?L��1H2SO4��0.01 mol?L��1����KMnO4��Һ��10%NaOH��Һ��10%H2O2��KSCN��Һ
| �������� | Ԥ������ͽ��� |
| ����1��ȡ������Ʒ���Թ��У�_________________ ____________________________________________ | ___________________________ |
| ����2�� ____________________________________________ | ___________________________ |
��4����ˮ���ա������������ա�ʱ�������Ȼ�������ɵõ����ᡣ����㣺��1000gˮ�����ձ�״���¶������Ȼ�������ɵõ�36.5%��Ũ�����д��������̣����������ѧ����ʽ��ʾ�����ػ���
��16�֣�
��1��Fe ��1�֣�
��2��FeCl2 + 2H2O Fe(OH)2 + 2HCl ��1�֣�
Fe(OH)2 + 2HCl ��1�֣�
4Fe(OH)2 + O2 +2H2O =" 4" Fe(OH)3 ��1�֣�
2Fe(OH)3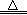 Fe2O3 + 3H2O ��1�֣�©д�������÷֣�
Fe2O3 + 3H2O ��1�֣�©д�������÷֣�
����4FeCl2+4H2O+O2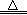 2 Fe2O3+8HCl ��3�֣�©д������2�֣�
2 Fe2O3+8HCl ��3�֣�©д������2�֣�
��3������1 ��1�֣�
������ÿ��2�֣���8�֣� ʵ����� Ԥ������ͽ��� ����1������������3mol?L��1H2SO4������� ��Ʒȫ���ܽ� ����2��ȡ������Һ���Թ��У������������ۣ�������ټ�������3mol?L��1H2SO4������� �Թ��г��ֺ�ɫ���壬˵����������CuO
������˵��������1��δ�ӡ��������͡��������1�֡�
����2�з���Ϊ��������10%NaOH��Һ�����������ɫ������˵����������CuO��������2�ͽ��۵�0�֣���Ϊ��Fe3+��H+���ţ���һ���ܹ۲쵽��ɫ������
����2 ��1�֣�ʵ����� Ԥ������ͽ��� ����1������������3mol?L��1H2SO4������� ��Ʒȫ���ܽ� ����2��ȡ������Һ���Թ��У���μ���0.01 mol?L��1����KMnO4��Һ ����Ϻ�ɫ��ȥ��˵����������FeO��
������˵��������1��δ�ӡ��������͡��������1�֡�
����2�У���KSCN��H2O2����ϼ���Fe2+������2�ͽ��۵�0�֣���Ϊ�� Fe3+���š�
��4����3�֣��������HCl���ΪxL����
(36.5x/22.4)/(1000+ 36.5x/22.4) ��100%=36.5% ��2�֡���ȷ��ʽ��2�֣�
���x= 22400/63.5(L)=352.89(L) ��1�֣�������ȷ�Ĵ�Ҳ�÷֣�
���������������1�����ݳ�ȥ�����ʲ�����������ԭ��Fe+2H+=Fe2++H2������˳��Ჽ��ѡ��ĵ���Xһ���ǹ��������ۻ���м����2���Ȼ�������ǿ�������Σ���ˮ�⣬����ˮ�ⷴӦ�����ȷ�Ӧ����˸�����ʹ�䳹��ˮ�⣬�����������������Ȼ��⣻�Ȼ��������ݳ����������������ȶ������ױ������е���������Ϊ����������������������ʱ�ֽ⣬������������ˮ����������������Ӧ���Եõ��ܷ�Ӧʽ����3��������1������Fe2O3��CuO����������ˮ�ļ������������ֱ��ѡ���Լ�����CuO�Ĵ��ڣ�������������ϡ�����ܽ����������������ͭ��Һ���ٸ��ݽ������˳��������Ρ�ͭ�ε����ʣ�Fe+Fe2(SO4)3=3FeSO4��Fe+CuSO4=FeSO4+Cu����˼�����������ۣ���ַ�Ӧ��������ɫ���壬˵����Ʒ�к���CuO����ѡ��NaOH��Һ��۲���Һ����ɫ�����У���Ϊ�����Ӷ�ͭ���ӵļ�����ɸ��ţ�������2������Fe2O3��FeO����������ˮ�ļ������������ֱ��ѡ���Լ�����FeO�Ĵ��ڣ�������������ϡ�����ܽ����������������������Һ���ٸ����Ρ������ε����ʣ�������Һ����ʹ���Ը��������Һ��ɫ������������Һ���ܣ���ӦΪ5Fe2++MnO4��+8H+=5Fe3++Mn2++4H2O����˼����������Ը��������Һ����ַ�Ӧ����Һ��ɫ��˵����Ʒ�к���FeO������ѡ��KSCN��˫��ˮ���飬��Ϊ�����ӻ�����������ӵļ��飻��4���������HCl���ΪxL������n=V/22.4L?mol��1��m=n?M��m(��Һ)=m(����)+m(ˮ)��w(����)=m(����)/m(��Һ)��100%����(36.5x/22.4)/(1000+ 36.5x/22.4) ��100%="36.5%" �����x= 22400/63.5(L)=352.8(L)��
���㣺���黯ѧ�������̴��⡢̽��ʵ������ƴ�̣��漰����Ԫ�ؼ��仯�������Ҫ���ʡ�����ˮ�⡢����Ħ����������ʵ��������������������ļ���ȡ�

���Ρ��������ڹ�ũҵ�����������ˮ�����ȷ������ż���㷺��Ӧ�á�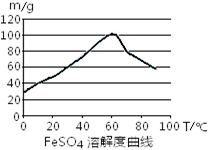
��1������м��ϡ���ᷴӦ�Ʊ�FeSO4
���Ʊ�ԭ�������ӷ���ʽ��ʾΪ ����Ҫ���FeSO4�������ʣ���ȡ���д�ʩ����ȷ���� ��
A��ʹ��Ũ��������м��Ӧ
B��ʹ��ĥϸ�����۷�Ӧ
C�������¶���50��70��
D�������¶���80��100��
����������Ӧ�����У�������淢����Ӧ��4Fe2++O2+4H+ 4Fe3++2H2O
4Fe3++2H2O
��Ҫ���ٲ�ƷFeSO4��Fe3+�ĺ�������ȡ���д�ʩ����ȷ���� ��
A������ϡ�����Ũ�Ȳ���̫��
B����ȥO2����ˮע��Ũ�������Ʒ�Ӧ�����ϡ����
C����Ӧ�б���n(Fe)/n(H2SO4) >1
D����Ӧ��Ӧ��������Fe2��SO4��3����
�۷�Ӧ��������Һ���� ����ȴ�����ˡ�ϴ�Ӽ���FeSO4��7H2O���塣
��2����ҵ���ú�������Cu��Al�ķ���м�Ʊ�Fe2��SO4��3
�䷴Ӧ�������������£�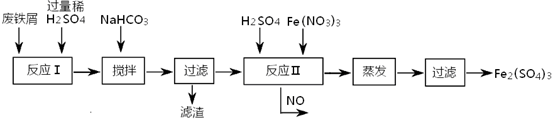
�ټ���NaHCO3�����裬�����ҺpH������ ��Χ�ڣ�ʹ���ʳ������˳�ȥ��
| ������ | Fe(OH)3 | Fe(OH)2 | Al(OH)3 | Cu(OH)2 |
| ��ʼ���� | 2.3 | 7.5 | 3.4 | 4.7 |
| ��ȫ���� | 3.2 | 9.7 | 4.4 | 6.7 |
�ڷ�Ӧ���з�Ӧ�����ӷ���ʽ�ǣ� ��
�������У�����Ӧ�������NO���һ������X����Ϻ�����ͨ�뷴Ӧ���У�����Ƶ�Ŀ���� ������X��NO��ȵı����� ��
��3����Fe2��SO4��3������S2-��ˮʱ���к�ɫ����������ɫ������������䷴Ӧ�����ӷ���ʽ�� ��
��������Fe3O4��ĩ���Ƴ����ȼ����ֳ����ȷݣ���һ��ֱ�ӷ����������ռ���Һ�У���ַ�Ӧ��ų������ڱ�״���µ����ΪV1����һ���ڸ�����ǡ�÷�Ӧ��ȫ����Ӧ��Ļ���������������ᷴӦ�ų��������ڱ�״���µ����ΪV2����һ��ֱ�ӷ��������������У���ַ�Ӧ��ų������ڱ�״���µ����ΪV3������˵����ȷ����
| A��V1=V3��V2 | B��V2��V1 =V3 | C��V1= V2��V3�� | D��V1��V3��V2 |
��������������Ԫ��֮һ�������Դٽ�Ѫ�쵰��������ӽ���������ҽѧ�Ͼ�����������������Ƭ����ƶѪ�IJ��˲��������������ҩƷ˵����ش����⣺
��1��ҩƬ�ϵ����¿�����__________�����ã�����ʱ�ܽ�������Ŀ����____________��
��2��ij�о�С�������KMnO4�ⶨFeSO4�ĺ�����
��ʵ��ǰ������Ҫ��ȷ����һ�����ʵ���Ũ�ȵ�KMnO4��Һ250����������ʱ��Ҫ��������������ƽ���ձ�������������Ͳ�⣬����Ҫ��������__________��___________��
�ڵζ�ʱ��������������Һ����___________�����������У����������Һ����__________�����������У��ζ�ʱ����___________�����̪�����ȡ���ʯ����üӡ���ָʾ��������жϴﵽ�ζ��յ�_____________��
��3����һ�о�С������������²���������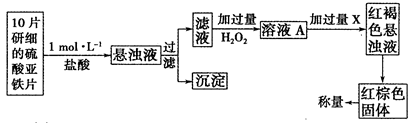
�ٴ˼�������мӹ���H2O2��Ӧ�����ӷ���ʽΪ______________��
�ڴӺ��ɫ������Һ�����ij����������������Ļ���������___________����������˳����д����
| A������ | B��ϴ�� | C����ȡ | D����Һ E����ȴ F������ |