题目内容
【题目】由有机物A和F合成I、J和高聚物H的流程如下:
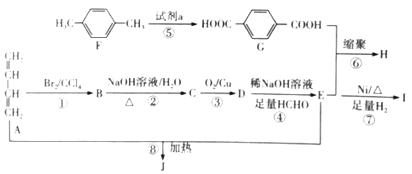
已知:①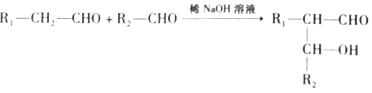
②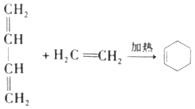
③有机物B的分子式为C4H6Br2,其核磁共振氢谱有2组峰,且峰面积之比为1:2。
请回答下列问题
(1)有机物F的名称是________,反应⑤利用试剂a的哪种性质? ________________填“氧化性”或“还原性”)。
(2)高聚物H的结构简式为_____________,已知J中含有一个六元环,则J的结构简式为________________。
(3)D→E的化学方程式为________________,反应类型为________________。
(4)1mol的E生成I最多可以消耗________molH2,B和C的相对分子质量的差值为________。
(5)C的同分异构体中满足下列条件的有________种。
①可以发生银镜反应 ②可以与金属钠反应产生氢气
【答案】 1,4-二甲苯或对二甲苯 氧化性 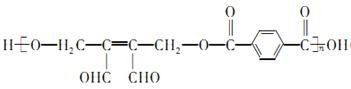
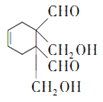
 加成反应 3 126 5
加成反应 3 126 5
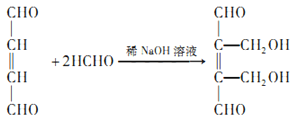
【解析】有机物B的分子式为C4H6Br2,其核磁共振氢谱有2组峰,且峰面积之比为1:2,故分子高度对称,A与溴发生1,4-加成生成B,B为1,4-二溴-2-丁烯BrCH2CH=CHCH2Br;BrCH2CH=CHCH2Br在氢氧化钠的水溶液中发生取代反应生成C为HOCH2CH=CHCH2OH,HOCH2CH=CHCH2OH在铜的催化下发生氧化反应生成D为OHCCH=CHCHO,OHCCH=CHCHO在稀氢氧化钠溶液中与足量甲醛发生类似已知①反应生成E为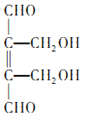 ,
,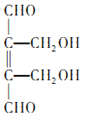 与A(1,3-丁二烯)发生类似已知②的加成反应生成J为
与A(1,3-丁二烯)发生类似已知②的加成反应生成J为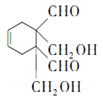 ,
,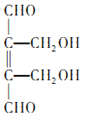 与G(对苯二甲酸)发生缩聚反应生成H为
与G(对苯二甲酸)发生缩聚反应生成H为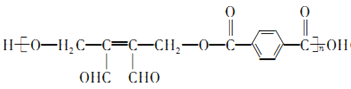 。(1)有机物F为
。(1)有机物F为![]() ,名称是1,4-二甲苯或对二甲苯,反应⑤是对二甲苯被酸性高锰酸钾溶液氧化生成对苯二甲酸,利用试剂a的氧化性;(2)高聚物H的结构简式为
,名称是1,4-二甲苯或对二甲苯,反应⑤是对二甲苯被酸性高锰酸钾溶液氧化生成对苯二甲酸,利用试剂a的氧化性;(2)高聚物H的结构简式为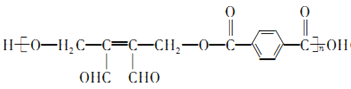 ,已知J中含有一个六元环,则J的结构简式为
,已知J中含有一个六元环,则J的结构简式为 ;(3)D→E是OHCCH=CHCHO在稀氢氧化钠溶液中与足量甲醛发生反应生成
;(3)D→E是OHCCH=CHCHO在稀氢氧化钠溶液中与足量甲醛发生反应生成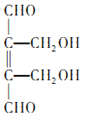 ,反应的化学方程式为
,反应的化学方程式为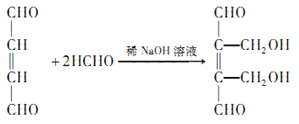 ,反应类型为加成反应;(4)
,反应类型为加成反应;(4)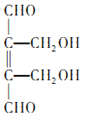 中含有一个碳碳双键和二个醛基,故1mol的E生成I最多可以消耗3molH2,B(BrCH2CH=CHCH2Br)和C(HOCH2CH=CHCH2OH)的相对分子质量的差值为80×2-17×2=126;(5)C为HOCH2CH=CHCH2OH,同分异构体中满足条件:①可以发生银镜反应则含有醛基,②可以与金属钠反应产生氢气,则另一个氧应是羟基,分子中不含有碳碳双键,符合条件的有CH3CH2CH(OH)CHO、(CH3)2C(OH)CHO、OHCCH2CH(OH)CH3、HOCH2CH(CH3)CHO、HOCH2CH2CHO共5种同分异构体。
中含有一个碳碳双键和二个醛基,故1mol的E生成I最多可以消耗3molH2,B(BrCH2CH=CHCH2Br)和C(HOCH2CH=CHCH2OH)的相对分子质量的差值为80×2-17×2=126;(5)C为HOCH2CH=CHCH2OH,同分异构体中满足条件:①可以发生银镜反应则含有醛基,②可以与金属钠反应产生氢气,则另一个氧应是羟基,分子中不含有碳碳双键,符合条件的有CH3CH2CH(OH)CHO、(CH3)2C(OH)CHO、OHCCH2CH(OH)CH3、HOCH2CH(CH3)CHO、HOCH2CH2CHO共5种同分异构体。

【题目】对利用甲烷消除NO2污染进行研究,CH4+2NO2![]() N2+CO2+2H2O。在1L密闭容器中,控制不同温度,分别加入0.50molCH4和1.2molNO2,测得n(CH4)随时间变化的有关实验数据见下表。
N2+CO2+2H2O。在1L密闭容器中,控制不同温度,分别加入0.50molCH4和1.2molNO2,测得n(CH4)随时间变化的有关实验数据见下表。
组别 | 温度 | 时间/min n/mol | 0 | 10 | 20 | 40 | 50 |
① | T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
② | T2 | n(CH4) | 0.50 | 0.30 | 0.18 | 0.15 |
下列说法正确的是( )
A. 由实验数据可知实验控制的温度T2>T1
B. 组别①中,0~20min内,NO2的降解速率为0.0125mol·L-1·min-1
C. 40min时,表格中T2对应的数据为0.18
D. 0~10min内,CH4的降解速率①>②