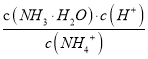题目内容
【题目】实验室以绿矾(FeSO4·7H2O)制备补血剂甘氨酸亚铁[(NH2CH2COO)2Fe] ,有关物质性质如下表所示:
物质 | 性质 |
甘氨酸(NH2CH2COOH) | 易溶于水,微溶于乙醇,两性化合物 |
柠檬酸 | 易溶于水和乙醇,有强酸性和还原性 |
甘氨酸亚铁 | 易溶于水,难溶于乙醇 |
实验过程:
Ⅰ.配制含0.10mol FeSO4的绿矾溶液。
Ⅱ.制备FeCO3 :将配制好的绿矾溶液与200mL 1.1mol·L-1NH4HCO3溶液混合,反应结束后过滤并洗涤沉淀。
Ⅲ.制备(NH2CH2COO)2Fe :实验装置如下图(夹持和加热仪器已省略),将实验Ⅱ得到的沉淀和含0.20 mol甘氨酸的水溶液混合后加入C中,然后利用A中的反应将C中空气排净,接着滴入柠檬酸溶液并加热。反应结束后过滤,滤液经蒸发结晶、过滤、洗涤、干燥得到产品。回答下列问题:

(1)仪器E的名称是_______________。
(2)实验I中:实验室配制绿矾溶液,将铁粉与稀硫酸混合时需要过量的试剂是______。
(3)实验II中:制备FeCO3时应向_______溶液中缓慢加入________溶液,并边加边搅拌,若颠倒试剂滴加顺序可能产生的后果是__________________。
(4)确认C中空气排尽的实验现象是______________。
(5)加入柠檬酸溶液一方面可调节溶液的pH促进FeCO3溶解,另一个作用是___________。
(6)洗涤实验Ⅲ中得到的沉淀,所选用的最佳洗涤试剂是_______________(填序号)。
A.热水 B.乙醇溶液 C.柠檬酸溶液
(7)若产品的质量为17.34g,则产率为________%。
【答案】长颈漏斗铁粉FeSO4NH4HCO3可能生成氢氧化亚铁沉淀D中澄清石灰水变浑浊防止二价铁被氧化B85
【解析】
(1)根据仪器构造可知,仪器E的名称是长颈漏斗,
故答案为:长颈漏斗;
(2)Fe2+易被空气中的O2氧化成Fe3+,实验室配制绿矾溶液时,为防止FeSO4被氧化变质,应加入的试剂为Fe,加入铁粉后,Fe3+可被铁粉还原为Fe2+且不引入杂质,
故答案为:铁粉;
(3)实验II中:制备FeCO3时应向配制好的绿矾溶液中缓慢加入200mL 1.1mol·L-1NH4HCO3溶液,并边加边搅拌,若颠倒试剂滴加顺序可能产生的后果是可能生成氢氧化亚铁沉淀,
故答案为:FeSO4 ;NH4HCO3 ;可能生成氢氧化亚铁沉淀;
(4)当C中充满CO2后,CO2开始进入D中,使D中的澄清石灰水变浑浊,这时说明C中空气已经排尽,
故答案为:D中澄清石灰水变浑浊;
(5)由题中信息可知,柠檬酸具有强还原性,还可防止Fe2+被氧化,
故答案为:防止二价铁被氧化;
(6)因甘氨酸亚铁易溶于水,难溶于乙醇,所以应选择乙醇溶液作为洗涤剂,故选B项。
故答案为:B。
(7)含0.10mol FeSO4的绿矾溶液中Fe2+的物质的量为0.10mol,因NH4HCO3溶液过量,所以根据Fe元素守恒,生成(NH2CH2COO)2Fe的物质的量为0.10mol、质量为20.4g,则产率为:![]() ×100%=85%。
×100%=85%。

 教材全解字词句篇系列答案
教材全解字词句篇系列答案【题目】①~⑧在元素周期表的对应位置如图所示,用化学式或元素符号回答下列问题。
族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
2 | ⑦ | ① | ② | |||||
3 | ③ | ④ | ⑤ | ⑧ | ⑥ |
(1)元素⑧的原子结构示意图__________;
(2)请写出⑦的单质与⑧的最高价氧化物对应的水化物的浓溶液在加热条件下反应的化学方程式为:__。
(3)元素③的最高价氧化物对应的水化物中含有_____(填离子键、极性共价键或非极性共价键),该物质的电子式为________
(4)元素①的氢化物与其最高价氧化物所对的水化物反应的产物为______,该物质为_______(填离子化合物或共价化合物);一定条件下①的氢化物与⑥的单质混合,得到另一种单质和盐的化学方程式为_________。
【题目】一定条件下反应A(g)+B(g)C(g)△H<0达到平衡后,据下列图象判断:

达到新的平衡对应的图象 (填写字母) | 平衡移动方向 (正反应、逆反应,不移动) | |
(i)使用催化剂 | _________ | ________ |
(ii)升温 | _________ | _________ |
(iii)降压 | _________ | _________ |
(iv)增加A的量 | __________ | _________ |
(v)减少C的量 | __________ | ________ |