题目内容
【题目】下列说法正确的是
A. 一定温度下,反应MgCl2(1)= Mg(1)+Cl2(g)的 △H>0,△S>0
B. 常温下,NH4Cl溶液加水稀释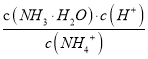 增大
增大
C. 电解饱和食盐水产生了11.2LH2,则反应中转移的电子数为6.02×1023
D. 在NaCl和KBr的混合溶液中滴加AgNO3溶液,一定先产生淡黄色沉淀
【答案】A
【解析】A项,该反应为分解反应,ΔH![]() 0,反应物中没有气体,生成物中有气体,ΔS
0,反应物中没有气体,生成物中有气体,ΔS![]() 0,正确;B项,NH4Cl溶液中存在水解平衡:NH4++H2O
0,正确;B项,NH4Cl溶液中存在水解平衡:NH4++H2O![]() NH3·H2O+H+,加水稀释促进NH4+的水解,
NH3·H2O+H+,加水稀释促进NH4+的水解, 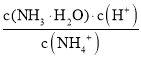 为水解平衡常数,温度不变,水解平衡常数不变,加水稀释
为水解平衡常数,温度不变,水解平衡常数不变,加水稀释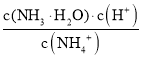 不变,错误;C项,没有指明H2所处温度和压强,无法计算11.2LH2的物质的量,无法计算转移的电子数;D项,由于NaCl和KBr的浓度未知,无法确定加入AgNO3溶液优先达到的是AgCl的溶度积还是AgBr的溶度积,无法确定优先生成AgCl沉淀还是AgBr沉淀,错误;答案选A。
不变,错误;C项,没有指明H2所处温度和压强,无法计算11.2LH2的物质的量,无法计算转移的电子数;D项,由于NaCl和KBr的浓度未知,无法确定加入AgNO3溶液优先达到的是AgCl的溶度积还是AgBr的溶度积,无法确定优先生成AgCl沉淀还是AgBr沉淀,错误;答案选A。

练习册系列答案
 怎样学好牛津英语系列答案
怎样学好牛津英语系列答案
相关题目
【题目】根据下列实验操作和现象得出的结论正确的是
选项 | 实验操作 | 现象 | 结论 |
A | 将某溶液与稀盐酸反应产生的气体通入澄 清 石灰 水 | 石灰水变浑浊 | 该溶液中一定含有CO32- |
B | 向某食盐溶液中滴加淀粉溶液 | 溶液颜色不变 | 该食盐中一定没有添加碘酸钾 |
C | 将乙烯通入溴的四氯化碳溶液 | 溶液最终变为无色透明 | 生成的1,2-二溴乙烷无色、可溶于四氯化碳 |
D | 向苯酚钠溶液中滴加乙酸溶液 | 溶液变浑浊 | 相同条件下,乙酸的酸性比苯酚强 |
A. A B. B C. C D. D