题目内容
【题目】将气体A、B置于固定容积为2 L的密闭容器中,发生如下反应:3A(g)+B(g)![]() 2C(g)+2D(g),反应进行到10 s末,达到平衡,测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
2C(g)+2D(g),反应进行到10 s末,达到平衡,测得A的物质的量为1.8 mol,B的物质的量为0.6 mol,C的物质的量为0.8 mol。
(1)用C表示10 s内反应的平均反应速率为________。
(2)反应前A的物质的量浓度是________。
(3)10 s末,生成物D的浓度为________。
(4)A与B的平衡转化率之比为________。
(5)平衡后,若改变下列条件,生成D的速率如何变化(填“增大”、“减小”或“不变”):
①降低温度____________;②增大A的浓度____________。
【答案】0.04 mol/(L·s) 1.5 mol/L 0. 4 mol/L 1∶1 减小 增大
【解析】
(1)根据v=![]() 表示反应速率;
表示反应速率;
(2)根据物质转化关系,由生成物C的物质的量计算反应消耗的A的物质的量,再结合10 s时剩余A的物质的量可得反应开始时A的物质的量,利用c=![]() 计算开始时A物质的浓度;
计算开始时A物质的浓度;
(3)根据方程式知,10 s末生成的n(D)=n(C)=0.8 mol,利用c=![]() 计算D的物质的浓度;
计算D的物质的浓度;
(4)根据C的物质的量计算反应消耗的A、B的物质的量,然后根据转化率等于![]() ×100%计算比较;
×100%计算比较;
(5)根据温度、浓度对化学反应速率的影响分析解答。
(1)反应从正反应方向开始,开始时C的物质的量为0,10 s时C的物质的量为0.8 mol,由于容器的容积是2 L,所以用C物质表示的10 s内化学反应平均反应速率v(C)=![]() =
=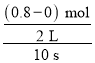 =0.04 mol/(L·s);
=0.04 mol/(L·s);
(2)根据反应方程式3A(g)+B(g)![]() 2C(g)+2D(g)可知:每反应消耗3 mol A就会同时产生2 mol C物质,10 s内反应产生了0.8 mol C,则反应消耗A的物质的量为△n(A)=
2C(g)+2D(g)可知:每反应消耗3 mol A就会同时产生2 mol C物质,10 s内反应产生了0.8 mol C,则反应消耗A的物质的量为△n(A)=![]() ×0.8 mol=1.2 mol,此时还有A物质1.8 mol,因此反应开始时A的物质的量是n(A)=1.8 mol+1.2 mol=3.0 mol,所以反应开始时A的浓度c(A)=
×0.8 mol=1.2 mol,此时还有A物质1.8 mol,因此反应开始时A的物质的量是n(A)=1.8 mol+1.2 mol=3.0 mol,所以反应开始时A的浓度c(A)=![]() =1.5 mol/L;
=1.5 mol/L;
(3)根据方程式知,10 s末生成的n(D)=n(C)=0.8 mol,则c(D)=![]() =0.4 mol/L;
=0.4 mol/L;
(4)根据已知条件可知:反应进行到10 s末C物质的量是0.8 mol,则反应消耗A的物质的量为△n(A)=![]() ×0.8 mol=1.2 mol,此时还有A物质1.8 mol,则反应开始时A的物质的量是n(A)=1.8 mol+1.2 mol=3.0 mol;△n(B)=
×0.8 mol=1.2 mol,此时还有A物质1.8 mol,则反应开始时A的物质的量是n(A)=1.8 mol+1.2 mol=3.0 mol;△n(B)=![]() ×0.8 mol=0.4 mol,此时还有B物质0.6 mol,所以反应开始时n(B)=0.6 mol+0.4 mol=1.0 mol,反应开始时n(A):n(B)=3:1,△n(A):△n(B)= 3:1,等于化学方程式中二者化学计量数的比,所以反应物A、B转化率相等,则两种物质反应时转化率的比为1:1;
×0.8 mol=0.4 mol,此时还有B物质0.6 mol,所以反应开始时n(B)=0.6 mol+0.4 mol=1.0 mol,反应开始时n(A):n(B)=3:1,△n(A):△n(B)= 3:1,等于化学方程式中二者化学计量数的比,所以反应物A、B转化率相等,则两种物质反应时转化率的比为1:1;
(5)①平衡后,若降低温度,物质的内能减小,活化分子数减少,分子之间有效碰撞次数减少,化学反应速率减小;
②平衡后,若增大反应物A的浓度,单位体积内活化分子数增加,分子之间有效碰撞次数增加,化学反应速率增大。

 同步轻松练习系列答案
同步轻松练习系列答案 课课通课程标准思维方法与能力训练系列答案
课课通课程标准思维方法与能力训练系列答案【题目】实验室制备1,2-溴乙烷的反应原理如下:CH3CH2OH![]() CH2=CH2+H2O CH2=CH2+Br2
CH2=CH2+H2O CH2=CH2+Br2![]() BrCH2CH2Br可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚。用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:
BrCH2CH2Br可能存在的主要副反应有:乙醇在浓硫酸的存在下在140℃脱水生成乙醚。用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:
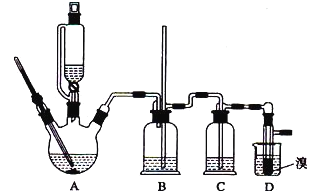
有关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | |
状态 | 无色液体 | 无色液体 | 无色液体 |
密度(g/cm3) | 0.79 | 2.2 | 0.71 |
沸点(℃) | 78.5 | 132 | 34.6 |
熔点(℃) | -130 | 9 | -116 |
回答下列问题:
(1)在此制备实验中,要尽可能迅速地把反应温度提高到170℃左右,其最主要目的是______(填正确选项前的字母)。
a.引发反应 b.加快反应速度 c.防止乙醇挥发 d.减少副产物乙醚生成
(2)装置B的作用是______。
(3)在装置c中应加入____(填正确选项前的字母),其目的是吸收反应中可能生成的酸性气体。
a.水 b.浓硫酸 c.氢氧化钠溶液 d.饱和碳酸氢钠溶液
(4)判断该制备反应己经结束的最简单方法是_______。
(5)将1, 2-二溴乙烷粗产品置于分液漏斗中加水,振荡后静置,产物应在____层(填“上”、“下”)。
(6)若产物中有少量未反应的Br2,最好用______(填正确选项前的字母)洗涤除去。
a.水 b.氢氧化钠溶液 c.碘化钠溶液 d.乙醇
(7)若产物中有少量副产物乙醚,可用________的方法除去。
(8)反应过程中应用冷水冷却装置D,其主要目的是_________;但又不过度冷却(如用冰水),其原因是______________________。