题目内容
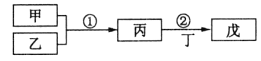
【题目】已知A与![]() 、CO形成B,B能发生银镜反应,C分子中只有一种氢,相关物质转化关系如下
、CO形成B,B能发生银镜反应,C分子中只有一种氢,相关物质转化关系如下![]() 含有相同官能团的有机物通常具有相似的化学性质
含有相同官能团的有机物通常具有相似的化学性质![]() :
:

请回答:
![]() 有机物C的结构简式是______,反应②的反应类型是______。
有机物C的结构简式是______,反应②的反应类型是______。
![]() 写出一定条件下发生反应①的化学方程式______。
写出一定条件下发生反应①的化学方程式______。
![]() 下列说法不正确的是______
下列说法不正确的是______![]() 填字母
填字母![]() 。
。
A.化合物A属于烃
B.化合物D含有两种官能团
C.用金属钠无法鉴别化合物F、G
【答案】![]()
![]()
![]()
![]()
【解析】
石蜡分解生成A,A与![]() 、CO形成B,B能发生银镜反应,根据B的分子式可知B为CH3CH2CHO,C分子中只有一种氢,则C为
、CO形成B,B能发生银镜反应,根据B的分子式可知B为CH3CH2CHO,C分子中只有一种氢,则C为![]() ,因此A为H2C=CH2,C与水发生加成反应生成D为HOCH2CH2OH,B氧化生成E为CH3CH2COOH,A与E发生加成反应生成G为CH3CH2CH2CH2COOH,D与E发生酯化反应生成F为CH3CH2COOCH2CH2OH,以此来解答。
,因此A为H2C=CH2,C与水发生加成反应生成D为HOCH2CH2OH,B氧化生成E为CH3CH2COOH,A与E发生加成反应生成G为CH3CH2CH2CH2COOH,D与E发生酯化反应生成F为CH3CH2COOCH2CH2OH,以此来解答。
(1)有机物C的结构简式是为![]() ,反应②的反应类型是加成反应,
,反应②的反应类型是加成反应,
故答案为:![]() ;加成反应;
;加成反应;
(2)一定条件下发生反应①的化学方程式为![]() ,
,
故答案为:![]() ;
;
(3)A. 化合物A为乙烯,属于烃,故A正确;
B. 化合物D只有一种官能团,为-OH,故B错误;
C. G含-COOH,F含-OH,羧基与单质钠反应速率更快,用金属钠能鉴别化合物F、G,故C错误;
故答案选BC。

 品学双优卷系列答案
品学双优卷系列答案 小学期末冲刺100分系列答案
小学期末冲刺100分系列答案 期末复习检测系列答案
期末复习检测系列答案 超能学典单元期中期末专题冲刺100分系列答案
超能学典单元期中期末专题冲刺100分系列答案【题目】醇脱水是合成烯烃的常用方法,实验室合成环己烯的反应和实验装置如下:


可能用到的有关数据如下:
物质 | 相对分子质量 | 密度/gcm-3 | 沸点/℃ | 溶解性 |
环己醇 | 100 | 0.9618 | 161 | 微溶于水 |
环己烯 | 82 | 0.8102 | 83 | 难溶于水 |
合成反应:在a中加入20g环己醇和2小片碎瓷片,冷却搅动下慢慢加入1mL浓硫酸。B中通入冷却水后,开始缓慢加热a,控制馏出物的温度不超过90℃。
分离提纯:反应粗产物倒入分液漏斗中分别用少量5%碳酸钠溶液和水洗涤,分离后加入无水氯化钙颗粒,静置一段时间后弃去氯化钙。最终通过蒸馏得到纯净环己烯10g。
回答下列问题:
(1)装置a、b的名称分别是__、__。
(2)加入碎瓷片的作用是__;如果加热一段时间后发现忘记加瓷片,应该采取的正确操作是__(填字母)。
A.立即补加 B.冷却后补加 C.不需补加 D.重新配料
(3)本实验中最容易产生的副产物的结构简式为__。
(4)分液漏斗在使用前须清洗干净并__;在本实验分离过程中,产物应该从分液漏斗的__(填“上口倒出”或“下口放出”)。
(5)分离提纯过程中加入无水氯化钙的目的是__。
(6)在环己烯粗产物蒸馏过程中,不可能用到的仪器有__(填字母)。
A.圆底烧瓶 B.温度计 C.吸滤瓶 D.球形冷凝管 E.接收器
(7)本实验所得到的环己烯产率是__(填字母)。
A.41% B.50% C.61% D.70%
【题目】X、Y、 Z三种可溶性盐,其阳离子分别是Ba2+、Cu2+、Ag+中的某一种,阴离子分别是Cl-、SO42-、NO3-中的某一种。现做以下实验:
①将三种盐各取少量,分别溶于盛有5 mL蒸馏水的三支试管中,只有X盐溶液呈蓝色。
②分别向三支试管中加入2 mL稀盐酸,发现Y盐溶液中产生白色沉淀,Z盐溶液无明显现象。
(1)根据上述事实,推断这三种盐的化学式:X______,Y______,Z______。
(2)若上述三种阳离子Ba2+、Cu2+、Ag+对应的盐都为硝酸盐,将其混合配成溶液,选择合适试剂,将这三种离子逐一沉淀分离。其流程图如下:

部分物质溶解性表为
Ba2+ | Cu2+ | Ag+ | |
Cl- | 溶 | 溶 | 不 |
CO32- | 不 | 不 | 不 |
SO42- | 不 | 溶 | 微 |
S2- | 溶 | 不 | 不 |
①沉淀1的化学式为_________________。
②写出混合溶液与试剂A反应的离子方程式:______________。
③若C为Na2S,且它与B的阳离子相同,则试剂B的名称是____________。
【题目】三硫代碳酸钠(Na2CS3)常用作杀菌剂、沉淀剂。某小组设计实验探究三硫代碳酸钠的性质并测定其溶液的浓度。
实验1:探究Na2CS3的性质
步骤 | 操作及现象 |
① | 取少量Na2CS3固体溶于蒸馏水配制成溶液并分成两等份 |
② | 向其中一份溶液中滴加几滴酚酞试液,溶液变红色 |
③ | 向另一份溶液中滴加酸性KMnO4溶液,紫色褪去 |
(1)H2CS3是___酸(填强或弱)。
(2)已知步骤③的氧化产物是SO42-,写出该反应的离子方程式___。
实验2:测定Na2CS3溶液的浓度,按如图所示连接好装置,取100mLNa2CS3溶液置于三颈烧瓶中,打开仪器d的活塞,滴入足量2.0mol/L稀H2SO4,关闭活塞。
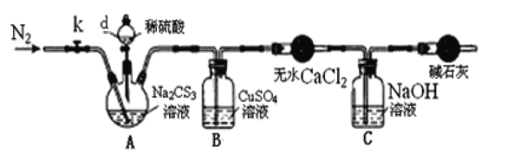
已知:Na2CS3+H2SO4=Na2SO4+CS2+H2S↑。CS2和H2S均有毒。CS2不溶于水,沸点46℃,与CO2某些性质相似,与NaOH作用生成Na2COS2和H2O。
(3)盛放无水CaCl2的仪器的名称是___。
(4)反应结束后打开活塞k,再缓慢通入热N2一段时间,其目的是___。
(5)为了计算Na2CS3溶液的浓度,对B中混合物进行过滤、洗涤、干燥、称重,得19.2g固体,则A中Na2CS3的物质的量浓度为___。(保留1位小数)