题目内容
6.一定量的气体在密闭容器中发生反应:xA(g)+yB(g)?zC(g),平衡时测得A的浓度为1.0mol•L-1,保持温度不变,将容器的容积扩大到原来的2倍,达到新平衡后,测得A的浓度降低为0.60mol•L-1.下列有关判断正确的是( )| A. | 平衡向正反应方向移动 | B. | 物质B的转化率降低 | ||
| C. | x+y<z | D. | 物质C的体积分数增大 |
分析 根据将容器的容积扩大到原来的两倍,若不考虑平衡移动,只考虑体积变化,A的浓度应变化为0.5mol/L,题干中再达到平衡时,测得A的浓度降低为0.60mol/L,说明体积增大,压强减小,平衡逆向进行,依据平衡移动方向分析判断选项中的问题.
解答 解:一定量的气体在密闭容器中发生反应:xA(g)+yB(g)?zC(g),平衡时测得A的浓度为1.0mol•L-1,将容器的容积扩大到原来的两倍,若不考虑平衡移动,只考虑体积变化,A的浓度应变化为0.5mol/L,题干中再达到平衡时,测得A的浓度降低为0.60mol/L.,说明体积增大,压强减小,平衡逆向进行;
A、平衡逆向进行,故A错误;
B、平衡逆向进行,B的转化率减小,故B正确;
C、体积增大,压强减小,化学平衡逆向进行,逆向是气体体积增大的反应,所以x+y>z,故以错误;
D、平衡逆向进行,C的体积分数减小,故D错误;
故选:B.
点评 本题考查化学平衡计算及化学平衡移动,明确体积变化引起A的浓度变化是解答本题的关键,注意动态变化与静态变化相结合得出平衡正向移动即可解答,题目难度不大.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
12.由-C6H5、-C6H4-、-CH2-、-OH四种原子团各一种组成属于酚类的物质的种类有( )
| A. | 3种 | B. | 4种 | C. | 1种 | D. | 2种 |
18.某烃含碳、氢元素的质量比为6:1,该径对氮气的相对密度为2,它即可使溴水褪色,又能与氢气加成,而与氢气的加成产物的有3种同分异构体,该径可以是( )
| A. | H2C=CH-CH2-CH3 | B. | 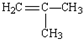 | C. | H2C=CH2 | D. |  |
15.几种微粒具有相同的核电荷数,则可说明( )
| A. | 可能是同一元素 | B. | 一定是同一元素 | ||
| C. | 彼此之间一定是同位素 | D. | 核外电子数一定相等 |
16.化学在生产和日常生活中有着重要的作用.下列有关说法正确的是( )
| A. | 二氧化硫有漂白性,常用作棉、麻、纸张和食品的漂白 | |
| B. | 大量使用化肥和农药,以提高农作物产量 | |
| C. | 汽车排放的尾气中含有NO、CO2等大气污染物 | |
| D. | 安装煤炭“固硫”装置,可以降低酸雨发生率 |
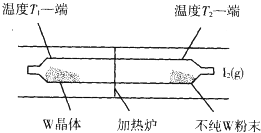 利用“化学蒸气转移法”提纯金属钨的反应原理为:W(s)+I2(g)?WI2(g)△H<0
利用“化学蒸气转移法”提纯金属钨的反应原理为:W(s)+I2(g)?WI2(g)△H<0
