题目内容
【题目】燃料电池是燃料(如氢气、甲烷、一氧化碳等)跟氧气(或空气)起反应将化学能转变为电能的装置,电解质溶液是强碱溶液。下面关于甲烷燃料电池的说法正确的是( )
A. 负极反应式:O2+2H2O+4e-![]() 4OH-
4OH-
B. 负极反应式:CH4+8OH--8e-![]() CO2+6H2O
CO2+6H2O
C. 随着放电的进行,溶液中氢氧根离子的浓度不变
D. 放电时溶液中的阴离子向负极移动
【答案】D
【解析】
燃料电池中,通入燃料的电极失电子发生氧化反应,电极反应式为:CH4+10OH--8e-═CO32-+7H2O,所以为负极,通入氧化剂的电极得电子发生还原反应,电极反应式为:2O2+4H2O+8e-═8OH-,所以为正极;所以电池反应式为:2O2+CH4+2OH-═CO32-+3H2O,根据总反应式判断溶液的pH变化;由电子的流向,判断溶液中离子的移动方向。
A.负极上CH4失电子发生氧化反应,故A错误;
B.燃料电池中,通入燃料的一极为负极,负极上失电子发生氧化反应,甲烷失电子生成二氧化碳和水,二氧化碳能和碱反应生成碳酸盐和水,所以负极电极反应式为:CH4+10OH--8e-═CO32-+7H2O,故B错误;
C.该电池反应式为2O2+CH4+2OH-═CO32-+3H2O,消耗了溶液中的氢氧根离子,且有溶剂水生成,导致溶液中氢氧根离子的浓度降低,故C错误;
D.放电时,电子从负极经外电路流向正极,溶液中的阳离子移向正极,阴离子移向负极,故D正确。
故选D。

 阳光课堂课时优化作业系列答案
阳光课堂课时优化作业系列答案【题目】X、Y、Z、W为按原子序数由小到大排列的四种短周期元素,已知:![]() 元素原子价电子排布式为
元素原子价电子排布式为![]() ,且原子半径是同族元素中最小的。
,且原子半径是同族元素中最小的。![]() 元素是地壳中含量最多的元素;W元素的电负性略小于Y元素,在W原子的电子排布中,p轨道上只有一个未成对电子。
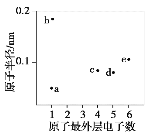
元素是地壳中含量最多的元素;W元素的电负性略小于Y元素,在W原子的电子排布中,p轨道上只有一个未成对电子。![]() 元素的电离能数据如表
元素的电离能数据如表![]() :
:
|
|
|
|
|
496 | 4562 | 6912 | 9540 |
|
请回答:
![]() 的电子式为______,含有的化学键类型为______,
的电子式为______,含有的化学键类型为______,![]() 为______晶体。
为______晶体。
![]() 遇水发生强烈水解产生一种气体A,溶液呈碱性,则A的结构式为______,其分子空间构型为______。
遇水发生强烈水解产生一种气体A,溶液呈碱性,则A的结构式为______,其分子空间构型为______。
![]() 、Y、Z、W四种元素所形成的单质中,硬度最大的是______
、Y、Z、W四种元素所形成的单质中,硬度最大的是______![]() 填物质的名称
填物质的名称![]() ;晶体
;晶体![]() 明显高的原因是______;
明显高的原因是______;![]() 中X原子的杂化轨道类型为______。
中X原子的杂化轨道类型为______。
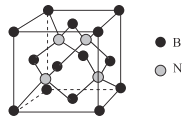
![]() 晶体的结构示意图如图所示。设该晶体的摩尔质量为
晶体的结构示意图如图所示。设该晶体的摩尔质量为![]() ,晶体的密度为
,晶体的密度为![]() 阿伏加德罗常数为
阿伏加德罗常数为![]() ,则晶体中两个最近的Z离子中心间的距离
,则晶体中两个最近的Z离子中心间的距离![]() ______。
______。