题目内容
2.实验室利用硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)制备聚铁(碱式硫酸铁的聚合物)和绿矾(FeSO4•7H2O),过程如下:
(1)将过程②中的产生的气体通入下列溶液中,溶液会褪色的是ACD;
A.品红溶液 B.紫色石蕊溶液 C.酸性KMnO4溶液 D.溴水
(2)过程③中,需加入的物质是Fe(或铁);
(3)过程⑤调节pH可选用下列试剂中的C (填选项序号);
A.稀硫酸 B.CaCO3 C.NaOH溶液
(4)过程⑥中,将溶液Z加热到70-80℃,目的是促进Fe3+的水解.
分析 硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)聚铁(碱式硫酸铁的聚合物)和绿矾(FeSO4•7H2O),烧渣在硫酸溶液中通入足量氧气,反应后过滤得到固体W和溶液X,溶液X加入铁反应生成硫酸亚铁,蒸发浓缩结晶析出得到绿矾,溶液X中加入试剂调节溶液PH得到溶液Z加热制备聚铁胶体得到聚铁;
(1)过程②产生的气体为SO2,具有还原性和漂白性;
(2)溶液X中含有Fe3+,要制备绿矾,应加入Fe使之还原为Fe2+;
(3)过程⑤调节pH应使溶液碱性增强,有利于聚铁的生成;
(4)过程⑥目的为促进的水解,加热有利于水解的进行.
解答 解:硫酸厂烧渣(主要成分为铁的氧化物及少量FeS、SiO2等)聚铁(碱式硫酸铁的聚合物)和绿矾(FeSO4•7H2O),烧渣在硫酸溶液中通入足量氧气,反应后过滤得到固体W和溶液X,溶液X加入铁反应生成硫酸亚铁,蒸发浓缩结晶析出得到绿矾,溶液X中加入试剂调节溶液PH得到溶液Z加热制备聚铁胶体得到聚铁;
(1)过程②产生的气体为SO2,具有还原性和漂白性,因具有漂白性而使品红褪色,因具有还原性而使具有氧化性的酸性KMnO4溶液、溴水褪色,故答案为:ACD;
(2)溶液X中含有Fe3+,要制备绿矾,应加入Fe使之还原为Fe2+,加入铁可生成Fe2+,并且不引入新的杂质,故答案为:Fe(或铁);
(3)过程⑤调节pH应使溶液碱性增强,有利于聚铁的生成,
A.加入硫酸不能使溶液PH增大,故A错误;
B.加入碳酸钙生成微溶的硫酸钙,会引入新的杂质,故B错误;
C.加入NaOH可使溶液碱性增强,生成的聚铁中不引入新的杂质,故C正确;
故答案为:C;
(4)过程⑥目的为促进的水解,加热有利于水解的进行,促进Fe3+的水解,故答案为:促进Fe3+的水解.
点评 本题考查较为综合,涉及水解的原理的应用、制备实验方案的设计等知识,题目难度较大,注意常见化学实验操作方法.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案| A. | 铁 | B. | 钙 | C. | 氧 | D. | 溴 |
(1)准确称取5.0g烧碱样品,将已称好的样品配成250mL待测液,需要的仪器除了烧杯,玻璃棒还有250mL容量瓶、胶头滴管.
(2)取10ml待测液于锥形瓶中,用0.2mol/L的标准盐酸滴定待测烧碱溶液,滴定时边滴边摇动锥形瓶,两眼注视锥形瓶内溶液的盐酸变化,直到滴定终点.
(3)判断到达滴定终点的实验现象是当滴入最后一滴盐酸,溶液由红色变为无色,且半分钟内不褪色.
| 滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) 滴定前读数(mL)滴定后读数(mL) | |
| 第一次 | 10.00 | 0.50 | 20.40 |
| 第二次 | 10.00 | 4.00 | 24.10 |
(5)下列操作会使实验结果偏低的是D
A.用蒸馏水洗净酸式滴定管后,即装入标准盐酸进行滴定
B.用蒸馏水洗净锥形瓶后,再用NaOH溶液润洗,后装入NaOH溶液进行滴定
C.用碱式滴定管取10.00mL NaOH溶液放入用蒸馏水洗净的锥形瓶中,再加入适量蒸馏水,最后用标准盐酸进行滴定
D.滴定过程中振荡锥形瓶时,有少量溶液洒在锥形瓶外面.
| A. | 酸式滴定管只用水洗 | |
| B. | 锥形瓶只用水洗 | |
| C. | 使用甲基橙做指示剂 | |
| D. | 第一次观察酸式滴定管的刻度时仰视 |

(1)蛇纹石矿加盐酸溶解后,溶液里除了Mg2+外,还含有的金属离子是Fe3+、Al3+;
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 9.4 |
(3)从沉淀混合物A中提取红色氧化物作颜料,先向沉淀物A中加入NaOH (填物质的化学式),然后过滤、洗涤、灼烧(依次填写实验操作名称).
 实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:请完成下列填空:
实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:请完成下列填空:(1)配制100mL 0.10mol/L NaOH标准溶液.
①主要操作步骤:计算→称量→溶解→(冷却后)转移→洗涤(并将洗涤液移入容量瓶)→定容→摇匀→将配制好的溶液倒入试剂瓶中,贴上标签.
②称量0.4g氢氧化钠固体所需仪器有:天平(带砝码、镊子)、药匙、烧杯.
(2)取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准NaOH溶液进行滴定.重复上述滴定操作2~3次,记录数据如下.
| 实验编号 | NaOH溶液的浓度 (mol/L) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测盐酸溶液的体积 (mL) |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.72 | 20.00 |
| 3 | 0.10 | 22.80 | 20.00 |
②根据上述数据,可计算出该盐酸的浓度约为0.11mol/L(保留两位有效数字)
③如图,排去碱式滴定管中气泡的方法应采用操作丙,然后轻轻挤压玻璃球使尖嘴部分充满碱液.
④在上述实验中,下列操作(其他操作正确)会造成测定结果偏高的有BD.(多选扣分)
A.滴定终点读数时俯视读数
B.碱式滴定管尖嘴部分有气泡,滴定后消失
C.锥形瓶水洗后未干燥
D.锥形瓶水洗后用待测稀盐酸溶液润洗
E.酸式滴定管使用前,水洗后未用待测盐酸溶液润洗.
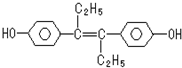
| A. | 该药物可以用有机溶剂萃取 | |
| B. | 可与NaOH反应但是不与Na2CO3发生反应 | |
| C. | 1mol该有机物不可以Br2发生取代反应 | |
| D. | 该有机物分子中,可能有16个碳原子共平面 |
