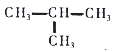题目内容
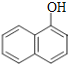
【题目】以苯酚为原料合成 ![]() 的路线如图所示。请按要求作答
的路线如图所示。请按要求作答

(1)写出苯酚制取A的有机物的有关反应方程式:______。
(2)写出以下物质的结构简式:B__________,F____________。
(3)写出反应④的化学反应方程式:④________,反应类型:_____。
(4)反应⑤可以得到E,同时可能得到的副产物的结构简式为_______。
(5)写出反应⑦的反应条件:__________,_________。
【答案】![]()
![]()
![]()
 +2NaOH
+2NaOH![]()
![]() +2NaBr+2H2O 消去反应
+2NaBr+2H2O 消去反应  、
、 NaOH水溶液 加热
NaOH水溶液 加热
【解析】
苯酚与H2发生加成反应生成的A为![]() ,A在浓硫酸并加热条件下反应生成的B能使溴水褪色,B的结构简式为
,A在浓硫酸并加热条件下反应生成的B能使溴水褪色,B的结构简式为![]() ;B与Br2发生加成反应生成C,C的结构简式为
;B与Br2发生加成反应生成C,C的结构简式为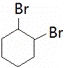 ,反应④的条件是氢氧化钠的乙醇溶液,则反应④为消去反应,D的结构简式为
,反应④的条件是氢氧化钠的乙醇溶液,则反应④为消去反应,D的结构简式为![]() ;由于最终产物是1,4-环己二醇,因此反应⑤是1,4-加成,E的结构简式为
;由于最终产物是1,4-环己二醇,因此反应⑤是1,4-加成,E的结构简式为![]() ;E通过加成反应生成F,F的结构简式为
;E通过加成反应生成F,F的结构简式为![]() ;据此分析作答;
;据此分析作答;
(1)苯酚与氢气发生加成反应,即反应①的方程式为![]() ;
;
(2)A在浓硫酸并加热条件下反应生成的B能使溴水褪色,B的结构简式为![]() ;B与Br2发生加成反应生成C,C的结构简式为
;B与Br2发生加成反应生成C,C的结构简式为 ,反应④的条件是氢氧化钠的乙醇溶液,则反应④为消去反应,D的结构简式为
,反应④的条件是氢氧化钠的乙醇溶液,则反应④为消去反应,D的结构简式为![]() ;由于最终产物是1,4-环己二醇,因此反应⑤是1,4-加成,E的结构简式为
;由于最终产物是1,4-环己二醇,因此反应⑤是1,4-加成,E的结构简式为![]() ;E通过加成反应生成F,F的结构简式为
;E通过加成反应生成F,F的结构简式为![]() ;
;
(3)根据上述分析,反应④的化学方程式为 +2NaOH
+2NaOH ![]()
![]() +2NaBr+2H2O,其反应类型为消去反应;
+2NaBr+2H2O,其反应类型为消去反应;
(4)反应⑤还有可能发生1,2-加成或全部加成,即副产物的结构简式为 、
、 ;
;
(5)F在NaOH的水溶液并加热条件下发生水解反应生成![]() ,即反应条件是NaOH水溶液、加热。
,即反应条件是NaOH水溶液、加热。

【题目】以废旧锌锰电池中的黑锰粉(MnO2、MnO(OH)、NH4Cl、少量ZnCl2及炭黑、氧化铁等)为原料制备MnCl2,实现锰的再利用。其工作流程如下:
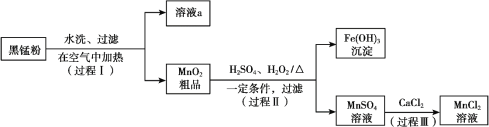
(1)过程Ⅰ,在空气中加热黑锰粉的目的是除炭、氧化MnO(OH)等。O2氧化MnO(OH)的化学方程式是_______。
(2)溶液a的主要成分为NH4Cl,另外还含有少量ZnCl2等。
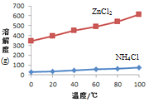
① 溶液a呈酸性,原因是______。
② 根据如图所示的溶解度曲线,将溶液a______(填操作),可得NH4Cl粗品。
③ 提纯NH4Cl粗品,有关性质数据如下:
化合物 | ZnCl2 | NH4Cl |
熔点 | 365℃ | 337.8℃分解 |
沸点 | 732℃ | ------------- |
根据上表,设计方案提纯NH4Cl:________。
(3)检验MnSO4溶液中是否含有Fe3+:取少量溶液,加入_______(填试剂和现象),证明溶液中Fe3+沉淀完全。
(4)探究过程Ⅱ中MnO2溶解的适宜条件。
ⅰ.向MnO2中加入H2O2溶液,产生大量气泡;再加入稀H2SO4,固体未明显溶解。
ⅱ.向MnO2中加入稀H2SO4,固体未溶解;再加入H2O2溶液,产生大量气泡,固体完全溶解。
① 用化学方程式表示ⅱ中MnO2溶解的原因:________。
② 解释试剂加入顺序不同,MnO2作用不同的原因:________。
上述实验说明,试剂加入顺序不同,物质体现的性质可能不同,产物也可能不同。
【题目】下列根据实验操作和现象所得出的结论正确的是
选项 | 实验操作 | 实验现象 | 结论 |
A | 将SO2气体通入酸性KMnO4溶液 | 溶液褪色 | SO2具有漂白性 |
B | 在CuSO4溶液中加入KI溶液,再加入苯,振荡 | 有白色沉淀产生,苯层呈紫红色 | Cu2+有氧化性,白色沉淀可能为CuI |
C | 向蛋白质溶液中分别加入甲醛、(NH4)2SO4饱和溶液 | 均有白色沉淀生成 | 蛋白质均发生了变性 |
D | 向5 mL 0.1 mol·L1 KI溶液中加入1 mL 0.1 mol·L1 FeCl3溶液,振荡,用苯萃取2~3次后,取下层溶液滴加5滴KSCN溶液 | 出现血红色 | 反应2Fe3++2I |
A.AB.BC.CD.D