题目内容
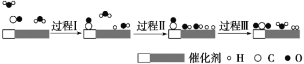
【题目】用如图所示实验装置进行物质性质的探究实验。下列说法不合理的是( )
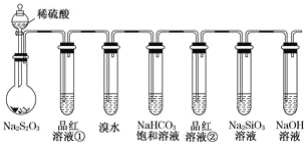
A.若品红溶液①褪色,则说明产物中含有SO2
B.若溴水褪色,则说明SO2具有还原性
C.若烧瓶中产生黄色浑浊和无色气泡,则说明Na2S2O3只作氧化剂
D.若品红溶液②不褪色、Na2SiO3溶液中出现白色浑浊,则说明硅酸比碳酸的酸性弱
【答案】C
【解析】
A.![]() 能使品红溶液褪色,故A合理;
能使品红溶液褪色,故A合理;
B.![]() 使溴水褪色,发生了氧化还原反应,二氧化硫被溴氧化为硫酸根离子,表现出
使溴水褪色,发生了氧化还原反应,二氧化硫被溴氧化为硫酸根离子,表现出![]() 的还原性,故B合理;
的还原性,故B合理;
C.Na2S2O3与硫酸发生歧化反应生成单质硫(黄色固体)和二氧化硫(刺激性气味气体),此反应中该物质既作氧化剂又作还原剂,故C不合理;
D.品红溶液②不褪色说明无![]() ,
, ![]() 溶液中出现白色浑浊,说明
溶液中出现白色浑浊,说明![]() 和
和![]() 饱和溶液反应产生了二氧化碳,依据强酸制弱酸的原理,说明硅酸比碳酸的酸性弱,故D合理。
饱和溶液反应产生了二氧化碳,依据强酸制弱酸的原理,说明硅酸比碳酸的酸性弱,故D合理。
故选C。

练习册系列答案
相关题目