题目内容
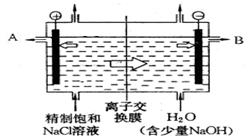
(10分)工业上电解制烧碱的技术是用离子交换膜法,主要原料是饱和食盐水。下图为离子交换膜法电解原理示意图:
请回答下列问题:
(1)电解槽中部的阳离子交换膜把电解槽隔成了阴极室和阳极室,这种阳离子交换膜,只允许溶液中的__________通过(填写下列微粒的编号),而两边的水不能自由流通。
①H+ ② Cl- ③Na+ ④OH-
(2)A极为电解槽的________极,电极反应式为__________________________________,
(3)如果没有阳离子交换膜,阴阳两极的某两种产物在常温下会在溶液中发生反应而使烧碱不纯,其反应的离子方程式为___________ 。
(4)若将标准状况下6.72L的阳极气体通入热的氢氧化钠溶液中,反应中只有一种元素的化合价发生改变,得到了两种含氯化合物,其中还原产物与氧化产物物质的量之比为5:1,写出该反应的离子方程式_____________________________________________。

请回答下列问题:
(1)电解槽中部的阳离子交换膜把电解槽隔成了阴极室和阳极室,这种阳离子交换膜,只允许溶液中的__________通过(填写下列微粒的编号),而两边的水不能自由流通。
①H+ ② Cl- ③Na+ ④OH-
(2)A极为电解槽的________极,电极反应式为__________________________________,
(3)如果没有阳离子交换膜,阴阳两极的某两种产物在常温下会在溶液中发生反应而使烧碱不纯,其反应的离子方程式为___________ 。
(4)若将标准状况下6.72L的阳极气体通入热的氢氧化钠溶液中,反应中只有一种元素的化合价发生改变,得到了两种含氯化合物,其中还原产物与氧化产物物质的量之比为5:1,写出该反应的离子方程式_____________________________________________。
(1)①③ (2)阳; 2Cl--2e-=Cl2↑
(3)Cl2 +2OH- Cl- +ClO- +H2O (4)3Cl2 +6OH-
Cl- +ClO- +H2O (4)3Cl2 +6OH- 5Cl- +ClO3- +3H2O
5Cl- +ClO3- +3H2O
(3)Cl2 +2OH-
 Cl- +ClO- +H2O (4)3Cl2 +6OH-
Cl- +ClO- +H2O (4)3Cl2 +6OH- 5Cl- +ClO3- +3H2O
5Cl- +ClO3- +3H2O试题分析:(1)阳离子交换膜只能允许阳离子通过,所以H+和Na+可以通过。
(2)根据阳离子的转移方向可知A极是阳极,B极是阴极,A极的电极反应为2Cl--2e-=Cl2↑。
(3)没有阳离子交换膜,Cl2可以与NaOH溶液反应,离子方程式为Cl2 +2OH-
 Cl- +ClO- +H2O。
Cl- +ClO- +H2O。(4)阳极气体是Cl2,与NaOH溶液反应时,只有一种元素的化合价变化,则说明发生了歧化反应,且还原产物与氧化产物物质的量之比为5:1,则生成了Cl-和ClO3-,所以反应的方程式为3Cl2 +6OH-
 5Cl- +ClO3- +3H2O。
5Cl- +ClO3- +3H2O。点评:电解中最关键的是准确判断出电极上离子的放电顺序。在判断电解产物时,首先判断阳极电极材料。如果是活性电极,则电极本身失去电子。如果是惰性电极,则溶液中的阴离子失去电子。而阴极是溶液中的阳离子得到电子,所以需要熟练记住常见离子的放电顺序。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
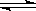 H++OH-,在不同温度下其平衡常数为K(25℃)=1.0×10-14,K(35℃)=2.1×10-14。则下列叙述不正确的是 ( )
H++OH-,在不同温度下其平衡常数为K(25℃)=1.0×10-14,K(35℃)=2.1×10-14。则下列叙述不正确的是 ( )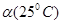 <
<