题目内容
18.有A、B、C三种短周期元素,A元素的原子半径是周期表中最小的元素,B元素的原子最外层电子书为4,C元素的原子最外层电子数次外层电子数的3倍,则这三种元素组成的化合物不可能是( )| A. | A2BC3 | B. | A4BC4 | C. | ABC4 | D. | A4B2C2 |
分析 有A、B、C三种短周期元素,A元素的原子半径是周期表中最小的元素,则A为H元素;B元素的原子最外层电子数为4,则B为碳或Si元素;C元素的原子最外层电子数次外层电子数的3倍,原子只能有2个电子层,最外层电子数为6,故C为O元素,结合常见化合物及元素化合价进行分析解答.
解答 解:有A、B、C三种短周期元素,A元素的原子半径是周期表中最小的元素,则A为H元素;B元素的原子最外层电子数为4,则B为碳或Si元素;C元素的原子最外层电子数次外层电子数的3倍,原子只能有2个电子层,最外层电子数为6,故C为O元素.
A.可以形成H2CO3或H2SiO3,故A正确;
B.可以形成H4SiO4,故B正确;
C.ABC4中B的化合价为+7,则B的最高化合价为+4,故C错误;
D.可以形成HOOC-COOH,故D正确,
故选C.
点评 本题考查了元素位置结构关系的应用,难度中等,能正确判断元素是解本题的关键,注意利用列举法解答.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
8.下列是一些制取物质的设计或设想,其中违背科学原理的是( )
| A. | 用玉米、植物秸杆等作原料制造乙醇,用作汽车的燃料 | |
| B. | 用动物的骨或皮作原料制造中药,用作滋补品 | |
| C. | 用淀粉作原料提取淀粉酶,用作催化剂 | |
| D. | 用植物油或动物脂肪作原料制造人造金刚石 |
9.已知:2NO2 ?N2O4△H<0,CaO溶于水放热,NH4Cl晶体溶于水吸热.在3个体积相等的圆底烧瓶中充满等量的NO2气体,并分别放置在加有下列物质的烧杯(烧杯内有水)中:(1)中加入CaO,(2)中加入NH4Cl晶体,(3)中不加任何其它物质,如图所示.下列叙述正确的是( )


| A. | (1)中红综色变深,(2)中红棕色变浅 | B. | (1)中红综色变浅,(2)中红棕色变深 | ||
| C. | 烧瓶(1)中气体的压强不变 | D. | 烧瓶(2)中气体的压强增大 |
6.下列有关电子排布图的表述正确的是( )
| A. |  可表示单核10电子粒子基态时电子排布 可表示单核10电子粒子基态时电子排布 | |
| B. |  此图错误,违背了泡利原理 此图错误,违背了泡利原理 | |
| C. | 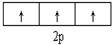 表示基态N原子的价电子排布 表示基态N原子的价电子排布 | |
| D. |  表示处于激发态的B的电子排布图 表示处于激发态的B的电子排布图 |
13.能一次区分乙酸、乙醇、苯、溴苯四种物质的是( )
| A. | 水 | B. | 碳酸氢钠溶液 | C. | 石蕊试液 | D. | 硫酸氢钠溶液 |
7.某科研单位利用石油裂解的副产物CH4来制取CO和H2,其生产流程如图1:
(1)该流程第Ⅰ步反应为:CH4(g)+H2O(g)?CO(g)+3H2(g),一定条件下CH4的平衡转化率与温度、压强的关系如图2.则P1<P2.(填“<”、“>”或“=”).该反应的平衡常数的表达式K=$\frac{c(CO){c}^{3}({H}_{2})}{c(C{H}_{4})c({H}_{2}O)}$.
(2)此流程的第Ⅱ步反应的平衡常数随温度的变化如表:
①从上表分析推断,该反应是△H<0(填“<”、“>”或“=”).
②在500℃时,设起始时CO和H2O的起始浓度均为0.010mol/L-1,在该条件下,反应达到平衡时,CO的转化率为75%.
③如图3表示该反应在t1时刻达到平衡,在t2时刻因改变某个条件浓度发生变化的情况:图中t2时刻发生改变的条件可能是降低温度,或增加水蒸汽的量,或减少氢气的量(写出两种).
(1)该流程第Ⅰ步反应为:CH4(g)+H2O(g)?CO(g)+3H2(g),一定条件下CH4的平衡转化率与温度、压强的关系如图2.则P1<P2.(填“<”、“>”或“=”).该反应的平衡常数的表达式K=$\frac{c(CO){c}^{3}({H}_{2})}{c(C{H}_{4})c({H}_{2}O)}$.
(2)此流程的第Ⅱ步反应的平衡常数随温度的变化如表:
| 温度/℃ | 300 | 500 | 830 |
| 平衡常数K | 12 | 9 | 1 |
②在500℃时,设起始时CO和H2O的起始浓度均为0.010mol/L-1,在该条件下,反应达到平衡时,CO的转化率为75%.
③如图3表示该反应在t1时刻达到平衡,在t2时刻因改变某个条件浓度发生变化的情况:图中t2时刻发生改变的条件可能是降低温度,或增加水蒸汽的量,或减少氢气的量(写出两种).

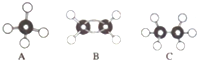
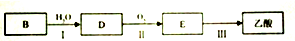
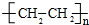
 高中化学教材介绍了钠、镁、铝、铁、氯、硫、氮、硅等元素及其化合物的知识,是学习研究其它化学知识的载体.
高中化学教材介绍了钠、镁、铝、铁、氯、硫、氮、硅等元素及其化合物的知识,是学习研究其它化学知识的载体.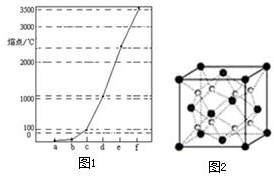 图1中a~f分别表示有H、C、N、Na、Si、Cu元素组成的单质,其中c、d均是热和电的良导体,单质分别对应的熔点如图所示:
图1中a~f分别表示有H、C、N、Na、Si、Cu元素组成的单质,其中c、d均是热和电的良导体,单质分别对应的熔点如图所示: