题目内容
下列实验报告记录的实验现象正确的是
| 实验 | 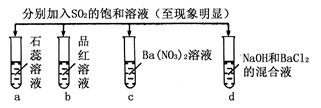 | ||||
| 记 录 | | a | b | c | d |
| A | 无色 | 不褪色 | 无色溶液 | 无色溶液 | |
| B | 红色 | 无色 | 白色沉淀 | 白色沉淀 | |
| C | 红色 | 无色 | 无色溶液 | 白色沉淀 | |
| D | 无色 | 无色 | 白色沉淀 | 无色溶液 | |
B
SO2溶于水显酸性,能使石蕊试液显红色。SO2有漂白性,但不能漂白酸碱指示剂,能使品红溶液褪色。SO2还具有还原性,在酸性溶液中能被硝酸钡氧化生成硫酸钡沉淀。在碱性溶液中,SO2能和氯化钡反应生成亚硫酸钡沉淀,答案选B。

练习册系列答案
 综合自测系列答案
综合自测系列答案
相关题目

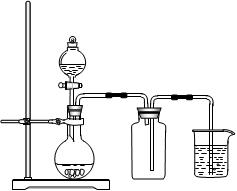



 (Fe) (b-a)×10-3L
(Fe) (b-a)×10-3L