题目内容
12.下列叙述正确的是( )| A. | 氧的摩尔质量为32 g/mol | |
| B. | 1 mol CO32-的质量为60 g/mol | |
| C. | H2SO4的摩尔质量等于H2SO4的相对分子质量 | |
| D. | 1 mol CO2的质量与CO2的相对分子质量在数值上相同 |
分析 A.没有指明是氧原子还是氧气分子;
B.g/mol为摩尔质量的单位,质量的常用单位为克;
C.H2SO4的相对分子质量为98,摩尔质量在数值上等于相对分子质量;
D.1 mol CO2的质量与CO2的相对分子质量在数值上同为44.
解答 解:A.必须指明粒子的具体名称,如氧气的摩尔质量为32g/mol,故A错误;
B.单位物质的量的物质所具有的质量称为摩尔质量.以g/mol为单位,在数值上,摩尔质量等于其相对分子质量,1 mol CO32-的质量为60 g,故B错误;
C.H2SO4的相对分子质量为98,H2SO4的摩尔质量M(H2SO4)=98g/mol,摩尔质量在数值上等于相对分子质量,故C错误;
D.1 molCO2质量为44g,CO2的相对分子质量为44,两者在数值上相同,故D正确;
故选D.
点评 本题考查了物质的量与摩尔质量的关系,题目难度不大,注意掌握摩尔质量、相对分子质量、物质的量的概念及表示方法.

练习册系列答案
相关题目
2.构成下列四种物质的微粒间,既存在离子键又存在共价键的是( )
| A. | MgCl2 | B. | K2S | C. | NaOH | D. | SO3 |
3.下列事实与氢键有关的是( )
| A. | 水加热到很高温度都难以分解 | |
| B. | 氨易液化,氨极易溶于水 | |
| C. | CH4、SiH4、GeH4、SnH4熔点随相对分子质量增大而升高 | |
| D. | HF、HCl、HBr、HI的热稳定性依次减弱 |
20.固体乙醇晶体中不存在的作用力是( )
| A. | 离子键 | B. | 氢键 | C. | 非极性键 | D. | 范德华力 |
7.某条件下,一定物质的量的铁和铝分别与足量盐酸反应,若生成气体的体积相同,则铁和铝的用量关系正确的是( )
| A. | 质量比为1:1 | B. | 质量之比为28:9 | ||
| C. | 物质的量之比为2:3 | D. | 物质的量之比为1:1 |
17.根据如图有关图象,说法正确的是( )
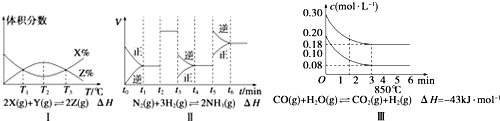

| A. | 由图Ⅰ知,反应在T1、T3处达到平衡,且该反应的△H<0 | |
| B. | 由图Ⅱ知,反应在t6时刻,NH3体积分数最大 | |
| C. | 由图Ⅱ知,t3时采取降低反应体系压强的措施 | |
| D. | 图Ⅲ表示在10 L容器、850℃时的反应,由图知,到4 min时,反应放出51.6 kJ的热量 |
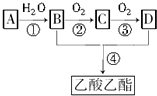
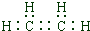 .
. CH3COOCH2CH3+H2O,属于取代反应.
CH3COOCH2CH3+H2O,属于取代反应.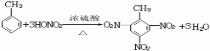 ,此反应属于取代反应,其生成物的名称是2.4.6-三硝基甲苯
,此反应属于取代反应,其生成物的名称是2.4.6-三硝基甲苯