题目内容
短周期元素X、Y、Z、Q在元素周期表中的相对位置如下图:地壳中含量最大的三种元素已包含其中。关于这些元素的叙述不合理的是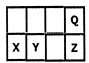
| A.最高价氧化物对应水化物的酸性Z>Y |
| B.原子半径X>Y |
| C.一定条件下,Q可分别与X、Y、Z形成化合物,这些化合物都可溶于NaOH溶液 |
| D.元素Y的氧化物是形成酸雨的罪魁祸首 |
D
解析试题分析:短周期元素中在地壳中含量按照由多到少的顺序排列前三种是O、Si、Al。由于最大的三种元素已包含其中。结合元素在周期表中的位置及结构可知:X是Al元素;Y是Si元素,Z是S元素,Q是O元素。A. 根据元素周期律可知:同周期的元素,随着原子序数的增加,元素的非金属性逐渐增强,则其最高价氧化物对应的水化物的酸性逐渐增强。所以最高价氧化物对应水化物的酸性Z>Y。正确。B.同周期的元素的原子半径随原子序数的增大而减小,所以原子半径X>Y。正确。C. O与Al、Si、S形成的化合物分别为Al2O3、SiO2、SO2和SO3。Al2O3是两性氧化物既能与酸反应又能与碱反应生成盐和水,而SiO2、SO2和SO3都是酸性氧化物,能与碱反应生成盐和水。正确。D.形成酸雨的罪魁祸首是SO2和NO2,与SiO2无关。错误。
考点:考查元素的推断及元素周期表、元素周期律、及元素和化合物的知识

根据不同的研究目的,可以编制成不同的元素周期表。将前18号元素按原子序数递增的顺序排列,可形成如图所示的“蜗牛”元素周期表,图中每个“.”代表一种元素,其中P点代表氢元素(图中的字母不表示元素符号)。下列说法正确的是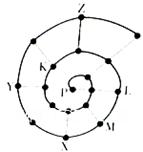
| A.Y点元素对应的氢化物比z点元素对应的氢化物更稳定 |
| B.虚线相连的两个点元索处于同一族 |
| C.比Y点原子序数小8的元素,它的最高氧化物对应的水化物是一种弱酸 |
D.K、L、X三种元素的离子半径大小顺序是X3+>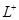 >K2- >K2- |
短周期元素X、Y、Z、W的原子序数依次增大,X原子的最外层电子数是其内层电子总数的3倍,Y原子的最外层只有2个电子,Z单质可制成半导体材料,W与X属于同一主族。下列叙述正确的是
| A.元素W的氢化物的稳定性比X的氢化物稳定性强 |
| B.元素Y的最高价氧化物对应水化物为强碱 |
| C.化合物YX、ZX2、WX2中化学键类型相同 |
| D.原子半径的大小顺序:rY>rZ>rW>rX |
门捷列夫制作元素周期表时,许多元素尚未发现,他在铝的下面留了空位给“类铝”,并对“类铝”的性质进行了预测, “类铝”与后来发现的镓的性质一致,从而验证了元素周期表的正确性。下列有关镓的性质的描述中错误的是
| A.镓的金属性比铝弱 | B.镓的常见化合价为+3 |
| C.镓的原子半径比铝大 | D.镓的原子结构示意图为 |
关于元素周期表的说法正确的是
| A.元素周期表中有8个主族 | B.元素周期表中有7个周期 |
| C.周期表中的主族都有金属元素 | D.IA族中的元素全部是金属元素 |
短周期元素的离子M2+和N2―具有相同的电子层结构,则下列说法正确的是
| A.M2+的离子半径比N2―小 | B.M的原子序数比N小 |
| C.M和N原子的电子层数相等 | D.M和N原子最外层电子数相等 |
下图是部分短周期元素原子半径与原子序数的关系图。则下列说法正确的是( )
| A.Z、N两种元素的离子半径相比,前者较大 |
| B.X、M两种元素的气态氢化物的稳定性相比,前者较弱 |
| C.由X与M两种元素组成的化合物不能与任何酸反应,但能与强碱反应 |
| D.Z的氧化物能分别溶解于Y的氢氧化物和N的氢化物的水溶液 |