题目内容
在下列各溶液中,离子一定能大量共存的是
| A.强酸性溶液中:K+、Al3+、CH3COO-、SO42- |
B.水电离出来的c(H+)=10-13mol/L的溶液:K+、HCO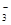 、Br-、Ba2+ 、Br-、Ba2+ |
| C.室温下,pH=1的无色溶液中:NH4+、Mg2+、SO42-、Cl- |
| D.室温下,pH=1的溶液中:Na+、Fe2+、NO3-、SO42- |
C
解析试题分析:A、在强酸性溶液中,醋酸根离子要与氢离子生成弱电解质醋酸,不能共存,错误;B、水电离出来的c(H+)=10-13mol/L的溶液,表明水的电离受到了抑制,不能共存,错误;C、正确;D、硝酸根离子在酸性条件下,可以氧化二价铁离子,不有共存,错误。
考点:考查离子共存。

练习册系列答案
相关题目
下列离子方程式正确的是
| A.Cl2通入水中:Cl2+H2O=2H+ +Cl-+ClO- |
| B.硫酸镁溶液与氢氧化钡溶液混合:SO42- + Ba2+ =BaSO4↓ |
C.用铜作电极电解CuSO4溶液:2Cu2++2H2O 2Cu+O2↑+4H+ 2Cu+O2↑+4H+ |
| D.AlCl3溶液中加入过量氨水:Al3++3NH3?H2O =Al(OH)3↓+ 3NH4+ |
下列离子方程式正确的是
| A.苯酚钠溶液中通入少量CO2:2C6H5O-+CO2+H2O→2C6H5OH+CO32- |
B.甲醛溶液中加入足量的银氨溶液并加热:HCHO+2[Ag(NH3)2]++2OH- HCOO-+NH4++2Ag↓+3NH3+H2O HCOO-+NH4++2Ag↓+3NH3+H2O |
C.乙醛与碱性氢氧化铜悬浊液混合后加热至沸腾:CH3CHO+2Cu(OH)2+OH— Cu2O↓+CH3COO—+3H2O Cu2O↓+CH3COO—+3H2O |
| D.向小苏打溶液中加入醋酸: CO32-+2CH3COOH =CO2↑+H2O+2CH3COO- |
下列离子方程式书写正确的是( )
| A.铝粉投入到NaOH溶液中:2Al+2OH-=2AlO2-+H2↑ |
| B.AlCl3溶液中加入足量的氨水:Al3++ 3OH-=Al(OH)3↓ |
| C.FeCl2溶液跟Cl2反应:2Fe2++Cl2=2Fe3++2Cl- |
| D.三氯化铁溶液中加入铁粉:Fe3+ + Fe = 2Fe2+ |
下列离子方程式书写正确的是
| A.氯化铁溶液中加入铜粉:2Fe3++Cu=== 2Fe2++Cu2+ |
| B.钠投入水中:Na+H2O===Na++2OH-+H2↑ |
| C.氯气和冷的氢氧化钠溶液反应:2Cl2+2OHˉ = 3Clˉ+ClOˉ+H2O |
| D.石灰石加入盐酸溶液中:2H+ + CO32–= CO2↑+H2O |
某溶液中可能存在Br-、CO32-、SO32-、Al3+、I-、Mg2+、Na+等7种离子中的某几种。现取该溶液进行实验,得到如下现象:
①向溶液中滴加足量氯水后,溶液变橙色,且有无色气泡冒出;
②向所得橙色溶液中加入足量BaCl2溶液,无沉淀生成;
③向所得溶液中继续滴加淀粉溶液,溶液不变蓝色。
据此可以推断:该溶液肯定不存在的离子组是
| A.Al3+、Mg2+、SO32- | B.Mg2+、CO32-、I- |
| C.Al3+、SO32-、I- | D.Al3+、Br-、SO32- |
下列离子方程式书写正确的是
| A.铝粉投入到NaOH溶液中:2Al+2OH-=2AlO2-+H2↑ |
| B.AlCl3溶液中加入足量的氨水:Al3++ 3OH-=Al(OH)3↓ |
| C.三氯化铁溶液中加入铁粉:Fe3++Fe=2Fe2+ |
| D.FeCl2溶液跟Cl2反应:2Fe2++Cl2=2Fe3++2Cl- |
在酸性溶液中,下列离子组在溶液中能大量共存的是
| A.Cu2+、NH4+、Br-、OH- | B.K+、Ba2+、OH-、SO42- |
| C.Ag+、NO3-、Cl-、K+ | D.Cl-、SO42-、K+、Na+ |
下列离子方程式书写正确的是( )
| A.将Na投入CH3COOH中:2Na+2H+=2Na++H2↑ |
B.将过量氨水加入到AlCl3溶液中:Al3++4OH-=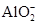 +2H2O +2H2O |
| C.向氯化银悬浊液中加入溴化钾溶液:Ag++Br-=AgBr↓ |
D.碳酸氢钙溶液中加入等物质的量的氢氧化钠溶液:Ca2++ 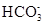 + OH-= CaCO3↓+H2O + OH-= CaCO3↓+H2O |